| 1. | V § 1 odstavec 2 včetně poznámky pod čarou č. 1a) zní: „(2) Odběr vzorků krmiv, doplňkových látek a premixů zahrnuje odběr dílčích vzorků pro účely sestavení souhrnného a konečného vzorku, odběr dílčích vzorků pro účely stanovení pracovní přesnosti míchacího zařízení a pro účely posouzení homogenity doplňkových látek a aminokyselin v premixech a krmivech s použitím premixů (dále jen „homogenita“) a způsob označování a uchovávání konečných, případně dílčích vzorků včetně vyhotovení protokolu o jejich odběru. Toto ustanovení se nevztahuje na odběr vzorků pro stanovení reziduí pesticidů a přítomnosti mikroorganismů, který se provádí podle zvláštního právního předpisu.1a) __________ 1a) | Vyhláška č. 294/1997 Sb., o mikrobiologických požadavcích na potraviny, způsobu jejich kontroly a hodnocení, ve znění vyhlášky č. 91/1999 Sb.„. |
|
| 2. | V § 2 se na konci odstavce 4 tečka vypouští a doplňují se slova „nebo pro posouzení pracovní přesnosti míchacích zařízení.“. |
| 3. | V § 2 se na začátek odstavce 6 vkládá nová věta, která zní: „Za vzorkovanou partii se považuje množství krmiva, doplňkové látky nebo premixu, které vykazuje jednotnost svým vnějším uspořádáním, označením a místním uložením.“. |
| 4. | V § 2 se doplňuje odstavec 7, který zní: „(7) Při odběru dílčích vzorků pro posouzení pracovní přesnosti míchacího zařízení se odebírá 10 dílčích vzorků z posuzovaného obsahu míchacího zařízení způsobem uvedeným v příloze č. 16.“. |
| 5. | V § 3 odst. 2 se za slova „s použitím premixu“ vkládají slova „nebo pro posouzení pracovní přesnosti míchacích zařízení“. |
| 6. | V § 3 se za odstavec 3 vkládá nový odstavec 4, který zní: „(4) Při odběru vzorků pro posouzení pracovní přesnosti míchacích zařízení tvoří dílčí vzorek odebraný z míchacího zařízení vždy jeden souhrnný vzorek, který je považován současně i za vzorek konečný.“. Dosavadní odstavec 4 se označuje jako odstavec 5. |
| 7. | V § 4 odstavec 1 zní: „(1) Ze souhrnného vzorku se přímo nebo po redukci vyhotoví nejméně tři konečné vzorky, které tvoří množství souhrnného vzorku určené pro zkoušení; minimální hmotnost konečného vzorku je uvedena v příloze č. 5 ve sloupci 2.“. |
| 8. | V § 4 odst. 2 se za slova „s použitím premixu“ vkládají slova „a pro posouzení pracovní přesnosti míchacího zařízení“. |
| 9. | V § 4 se doplňuje odstavec 4, který včetně poznámky pod čarou č. 4) zní: „(4)Vzorky určené k laboratornímu zkoušení se neprodleně doručí spolu s protokolem o odběru vzorku do příslušné laboratoře.4) _________ 4) | § 17 zákona č. 91/1996 Sb., o krmivech.“. |
|
| 10. | V § 5 se doplňují odstavce 4 až 6, které znějí: „(4) Ustanovení odstavců 1, 2 a 3 se nevztahuje na dílčí vzorky odebrané pro posouzení homogenity a pracovní přesnosti míchacích zařízení. (5) Při odběru dílčích vzorků pro posouzení homogenity nebo pracovní přesnosti míchacích zařízení se dílčí vzorky, které jsou i konečnými vzorky, uchovávají v čistých, suchých, vlhkost nepropouštějících, vzduchotěsně uzavíratelných obalech. Obaly se vzorky se uzavřou a označí vždy těmito údaji: a) | názvem vzorkovaného krmiva, doplňkové látky, premixu nebo u vzorků pro posouzení pracovní přesnosti ověřovaným typem míchacího zařízení, | b) | obchodním jménem a sídlem právnické osoby nebo jménem a příjmením fyzické osoby, která je výrobcem krmiva, doplňkové látky a premixu, u vzorků pro posouzení pracovní přesnosti obchodním jménem a sídlem právnické osoby nebo jménem a příjmením fyzické osoby, která je majitelem míchacího zařízení, | c) | jménem a příjmením fyzické osoby, která prováděla odběr vzorků. | (6) | Při odběru vzorků krmiv, doplňkových látek a premixů určených pro zkoušení fotolabilních látek se musí konečné vzorky uchovávat v obalech, které zabrání přístupu světla.“. |
|
| 11. | V § 6 odstavec 1 zní: „(1) O každém odběru konečného vzorku krmiva, doplňkové látky a premixu se vyhotoví protokol, který umožní přesnou identifikaci každé vzorkované partie tak, aby nemohlo dojít k záměně vzorků. Protokol o odběru vzorku se připojí ke každému konečnému vzorku. Pro účely posouzení homogenity nebo pracovní přesnosti míchacích zařízení se o odběru všech vzorků pořizuje pouze jeden protokol.“. |
| 12. | V § 7 se doplňuje odstavec 3, který zní: „(3) Pokud není metoda pro zkoušení daného znaku uvedena v přílohách č. 7 až 14 a kontrola tohoto znaku je nezbytná, lze použít jinou vhodnou metodu, která odpovídá dosažené úrovni vědeckého a technického poznání. Obecné podmínky pro použití zkušební metody jsou uvedeny v příloze č. 15.“. |
| 13. | V § 9 odstavec 1 zní: „(1) Zkušební vzorky krmiv, doplňkových látek a premixů se po skončení zkoušek uchovávají způsoby uvedenými v příloze č. 8.“. |
| 14. | V § 10 odstavec 3 zní: „(3) Koncentrace roztoků se vyjadřuje buď v hmotnostních nebo objemových procentech, nebo se vyjadřuje jako koncentrace látková (mol/l) nebo hmotnostní (mg/l, mg/ml).“. |
| 15. | § 11 zní: „§ 11 (1) Výsledkem chemické zkoušky krmiva, doplňkové látky nebo premixu je průměrná hodnota získaná nejméně ze dvou analýz provedených na dvou navážkách vzorku, pokud se výsledek analýz neodchyluje o větší hodnotu, než je hodnota meze opakovatelnosti /r/ (dále jen „opakovatelnost“), uvedená v přílohách č. 9 a 10. (2) Opakovatelnost je hodnota, o které lze předpokládat, že s pravděpodobností 95 % bude nižší nebo rovna absolutní hodnotě rozdílu mezi dvěma výsledky zkoušek získaných za podmínek opakovatelnosti. Podmínky opakovatelnosti jsou podmínky, kdy se nezávislé výsledky zkoušek získají stejnou metodou, na identickém materiálu, v téže laboratoři, týmž pracovníkem, za použití téhož vybavení, během krátkého časového rozmezí. (3) Není-li hodnota opakovatelnosti uvedena, vypočítá se postupem uvedeným v bodě 8 přílohy č. 15. (4) Výsledek chemické zkoušky se vyjadřuje v jednotkách uvedených v přílohách č. 9 až 14. Při stanovení původní vlhkosti krmiva, doplňkové látky nebo premixu se výsledky přepočítávají na původní sušinu. (5) Není-li u metody uvedeno jinak, vyjadřují se výsledky po zaokrouhlení takto: pro vyjádření obsahu v jednotkách mg/kg: pro obsah do 9,99 mg/kg | s přesností na 0,01 mg/kg | pro obsah od 10,0 do 99,9 mg/kg | s přesností na 0,1 mg/kg | pro obsah od 100 do 999 mg/kg | s přesností na 1 mg/kg | pro obsah od 1000 do 9999 mg/kg | s přesností na 10 mg/kg | pro obsah od 10000 do 99999 mg/kg | s přesností na 100 mg/kg | pro obsah nad 100 000 mg/kg | s přesností na 1000 mg/kg |
pro vyjádření obsahu v jednotkách g/kg: pro obsah do 9,99 g/kg | s přesností na 0,01 g/kg | pro obsah od 10 g/kg do 99,9 g/kg | s přesností na 0,1 g/kg | pro obsah nad 100 g/kg | s přesností na 1 g/kg. |
(6) Mez reprodukovatelnosti /R/ (dále jen „reprodukovatelnost“) je hodnota, o níž lze předpokládat, že s pravděpodobností 95 % bude nižší nebo rovna absolutní hodnotě rozdílu mezi dvěma výsledky zkoušek získaných za podmínek reprodukovatelnosti. Podmínky reprodukovatelnosti jsou podmínky, kdy se nezávislé výsledky zkoušek získají stejnou metodou, na indentickém materiálu v různých laboratořích, různými pracovníky, používajících různá vybavení. Reprodukovatelnost nezahrnuje chybu odběru vzorku. (7) Hodnoty reprodukovatelnosti pro jednotlivé metody zkoušení jsou uvedeny v přílohách č. 9, 10 a 17. Není-li hodnota reprodukovatelnosti stanovena, vypočítá se postupem uvedeným v bodě 8 přílohy č. 15.“. |
| 16. | § 12 zní: „§ 12 Zkoušení homogenity2) doplňkových látek a aminokyselin v partii premixu nebo krmiv s použitím premixů se provádí pomocí doplňkové látky nebo přidané aminokyseliny. Při posuzování pracovní přesnosti míchacího2) zařízení se používá doplňková látka, která při laboratorním zkoušení vykazuje nejnižší hodnotu opakovatelnosti a reprodukovatelnosti pro ověřovaný obsah.“. |
| 17. | V příloze č. 2 nadpis tabulky včetně vysvětlivky na konci přílohy zní: „Minimální počty dílčích vzorků *) Materiály se rozumí krmiva, doplňkové látky a premixy. __________ *) | Nevztahuje se na vzorkovanou partii, pokud počet obalů nebo hmotnost nebo objem je nižší, než je uvedeno v tabulce.“. |
|
| 18. | V příloze č. 2 bodě 1. se slova „Pevná krmiva“ nahrazují slovy „Pevné materiály“. |
| 19. | V příloze č. 2 bodě 2. se slova „Pevná krmiva balená do obalů:“ nahrazují slovy „Pevné materiály balené do obalů:“. |
| 20. | V příloze č. 2 bodě 3. se slova „Tekutá a polotekutá krmiva:“ nahrazují slovy „Tekuté a polotekuté materiály:“. |
| 21. | V příloze č. 3 nadpis tabulky včetně vysvětlivky na konci přílohy zní: „Minimální hmotnost souhrnného vzorku*) __________ *) | Nevztahuje se na vzorkovanou partii, pokud počet obalů nebo hmotnost nebo objem je nižší, než je uvedeno v tabulce.“. |
|
| 22. | Příloha č. 5 zní: „Příloha č. 5 k vyhlášce č. 222/1996 Sb. Minimální hmotnost konečného vzorku*) Druh a rozsah partie | | Minimální hmotnost konečného vzorku | 1 | | 2 | 1. Pevná krmiva | | 0,5 kg | 2. Tekutá a polotekutá krmiva | | 0,5 l | 3. Doplňkové látky | | 0,05 kg | 4. Premixy | | 0,25 kg. |
*) | Nevztahuje se na vzorkovanou partii, pokud počet obalů nebo hmotnost nebo objem je nižší, než je uvedeno v tabulce.“. |
|
| 23. | Nadpis přílohy č. 6 zní: „Postup odběru vzorků krmiv, doplňkových látek a premixů“. |
| 24. | V příloze č. 6 bodě 1. první věta zní: „Dílčí vzorky s výjimkou dílčích vzorků pro stanovení přítomnosti a obsahu nežádoucích látek, zakázaných látek a produktů, jakož i dílčích vzorků pro stanovení homogenity a posouzení pracovní přesnosti míchacích zařízení se odebírají nahodile tak, aby zahrnovaly celou vzorkovanou partii.“. |
| 25. | V příloze č. 6 se za bod 4. doplňují body 5. a 6., které znějí: „5. | Dílčí vzorky pro posouzení homogenity partie se odebírají z nahodile vybraných obalů nebo u volně ložených krmiv z nahodile vybraných míst, které jsou rovnoměrně rozloženy po celé vzorkované partii. Počet odebíraných dílčích vzorků z partie je uveden v příloze č. 14. | 6. | Dílčí vzorky pro posouzení pracovní přesnosti míchacího zařízení se odebírají tak, aby jejich odběr byl rovnoměrně rozmístěn po celé ploše prostoru míchacího zařízení nebo při vzorkování mimo míchací prostor byl rovnoměrně rozložen podle počtu vzorkovaných obalů nebo vzorkované hmotnosti.“. |
|
| 26. | V příloze č. 7 bodě 1. 2. se na konci druhého odstavce doplňuje tato věta: „Toto ustanovení se nevztahuje na konečné vzorky pro posouzení obsahu nežádoucích látek, homogenity a pracovní přesnosti míchacího zařízení.“. |
| 27. | V příloze č. 7 se za bod 1. 5. doplňují body 1. 6. a 1. 7., které znějí: „1. | 6. Konečné vzorky pro posouzení obsahu nežádoucích látek se předem smyslově posoudí, provedou se případné fyzikální a speciální zkoušky a konečný vzorek se jako celek upravuje tak, aby částice propadly drátěným sítem o velikosti strany oka 1 mm, a poté se dokonale promíchá tak, aby navážky požadované pro jednotlivé zkoušky byly homogenní a reprezentovaly konečný vzorek. Z takto upraveného vzorku se připravují navážky pro jednotlivé zkoušky. | 1. | 7. Konečné vzorky pro posouzení homogenity a pro posouzení pracovní přesnosti míchacího zařízení se nejprve jako celek upravují tak, aby částice propadly drátěným sítem o velikosti strany oka 1 mm, a poté se dokonale promíchají tak, aby navážky pro jednotlivé zkoušky byly homogenní a reprezentovaly konečný vzorek. Z takto upravených vzorků se připravují navážky pro jednotlivé zkoušky.“. |
|
| 28. | Příloha č. 9 zní: „Příloha č. 9 k vyhlášce č. 222 /1996 Sb. : Postupy pro laboratorní zkoušení krmiv, doplňkových látek a premixů Seznam postupů chemického zkoušení krmiv Název postupu | Označení postupu | 1. | Vlhkost, těkavé látky | | 1.1. | Stanovení obsahu vlhkosti v krmivech | | 1.2. | Stanovení obsahu vlhkosti a těkavých látek v tucích | -A- | 1.3. | Stanovení obsahu vlhkosti a těkavých látek v olejnatých semenech | -A- | 1.4. | Stanovení obsahu vlhkosti | -B- | 1.5. | Stanovení obsahu vlhkosti v olejích a tucích | -B- | | | | 2. | Dusíkaté sloučeniny | | 2.1. | Stanovení obsahu dusíkatých látek | -A- -B- | 2.2. | Stanovení obsahu dusíkatých látek rozpustných působením roztoku pepsinu v kyselině chlorovodíkové | -A- -B- | 2.3. | Stanovení obsahu bílkovin | -A- -B- | 2.4. | Stanovení obsahu aminokyselin | -B- | 2.5. | Stanovení obsahu močoviny | -A- -B- | 2.6. | Stanovení obsahu amoniaku v rybích moučkách | -A- -B- | 2.7. | Stanovení obsahu těkavých dusíkatých látek | -A- -B- | 2.8. | Stanovení aktivity ureázy v sóji a jejích produktech | -A- -B- | 2.9. | Ureázový test | -A- | 2.10. | Stanovení. obsahu biuretu | -A- | 2.11. | Stanovení obsahu hydroxyanalogu methioninu | -A- | 2.12. | Stanovení obsahu dusíkatých látek rozpustných působením pepsinu | -B- | 2.13. | Stanovení aktivity pepsinu | -B- | 2.14. | Stanovení obsahu methioninu | -A- | 2.15. | Stanovení obsahu tryptofanu | -A- -B- | | | | 3. | Tuk | | 3.1 | Stanovení obsahu tuku | -A- | 3.2. | Stanovení obsahu tuku v olejnatých semenech | -A- | 3.3. | Stanovení čísla kyselosti tuku | -A- | 3.4. | Stanovení obsahu lecitinu | -A- | 3.5. | Stanovení obsahu nerozpustných nečistot v tucích a olejích | -A- | 3.6. | Stanovení obsahu nezmýdelnitelných látek v tucích a olejích | -A- | 3.7. | Stanovení peroxidového čísla | -A- | 3.8. | Stanovení obsahu oleje a tuku | -B- |
4. | Polysacharidy | | 4.1. | Stanovení obsahu vlákniny | -A- -B- | | | | 5. | Bezdusíkaté látky výtažkové | | 5.1. | Stanovení obsahu škrobu | -A- -B- | 5.2. | Stanovení obsahu škrobu - pankreatický postup | -B- | 5.3. | Stanovení obsahu cukrů | -A- -B- | 5.4. | Stanovení obsahu laktosy | -A- -B- | 5.5. | Stanovení obsahu bezdusíkatých látek výtažkových výpočtem | -A- | 5.6. | Stanovení obsahu cukrů polarizací | -A--B- | 5.7. | Stanovení obsahu redukujících látek v cukru a melase | -A- | | | | 6. | Popel | | 6.1. | Stanovení obsahu popele | -A- -B- | 6.2. | Stanovení obsahu popele v tucích | -A- | 6.3. | Stanovení obsahu nerozpustného podílu popele v kyselině chlorovodíkové | -A- -B- | 6.4. | Stanovení obsahu popele nerozpustného v kyselině chlorovodíkové | -B- | | | | 7. | Makroprvky | | 7.1. | Stanovení obsahu fosforu | -A- -B- | 7.2. | Stanovení obsahu vápníku | -A- -B- | 7.3. | Stanovení obsahu hořčíku | -A- -B- | 7.4. | Stanovení obsahu draslíku | -A- -B- | 7.5. | Stanovení obsahu sodíku | -A- -B- | 7:6. | Stanovení obsahu ve vodě rozpustných chloridů | -A- -B- | 7.7. | Stanovení obsahu celkových uhličitanů | -A- -B- | 7.8. | Stanovení obsahu oxidů křemíku, hliníku; vápníku a hořčíku ve (vápencích) | -A- | 7.9. | Stanovení celkového obsahu síry | -A- -B- | 7.10. | Stanovení obsahu vápníku | -B- |
8. | Mikroprvky | | 8.1. | Stanovení obsahů mědi, železa, manganu a zinku | -A- | 8.2. | Stanovení obsahu vápníku, mědi, železa, hořčíku, manganu, draslíku, sodíku a zinku | -B- | 8.3. | Stanovení obsahu železa, mědi; manganu a zinku | -B- | | | | 9. | Kyselost | | 9.1. | Stanovení volné, vázané a celkové kyselosti vodního výluhu | -A- | 9.2. | Stanovení kyselosti vodního výluhu v mléčných krmných směsích | -A- | | | | 10. | Nežádoucí látky | | 10.1. | Stanovení obsahu kyanovodíku | -B- | 10.2. | Stanovení obsahu hořčičného oleje vyjádřeného jako allylisothiokyanát | -B- | 10.3. | Stanovení obsahu theobrominu | -B- | 10.4. | Stanovení obsahu glukosinolátů v řepce | -A- -B- | 10.5. | Stanovení obsahu 5-vinyl-2-thiooxazolidonu | -A- -B- | 10.6. | Stanovení obsahu kyseliny erukové | -A- | 10.7. | Stanovení obsahu olova a kadmia | -A- | 10.8. | Stanovení obsahu ricinových slupek | -A- -B- | 10.9. | Stanovení obsahu fluoru | -B- | 10.10. | Stanovení obsahu rezidují organochlorových a organofosfátových pesticidů | -B- | 10.11. | Stanovení obsahu hexachlorbenzenu | -B- | 10.12. | Stanovení obsahu dusitanů | -B- | 10.13. | Stanovení obsahu rtuti | -A- | 10.14. | Stanovení obsahu aflatoxinu B1 | -B- | 10.15. | Stanovení obsahu arsenu | -B- | 10.16. | Stanovení obsahu gossypolu | -B- | 10.17. | Stanovení obsahu theobrominu | -A- | | | | 11. | Zkoušení siláží | | 11.1. | Zkoušení jakosti siláží | -A- -B- |
1. | | Vlhkost, těkavé látky | | 1.1. | Stanovení obsahu vlhkosti v krmivech | | | Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vlhkosti v krmivech, premixech a doplňkových látkách. Postup je použitelný pro stanovení obsahu vlhkosti ve všech druzích krmiv, premixů a doplňkových látek s vyjímkou mléka a mléčných výrobků a olejnatých semen. Obsah vlhkosti se stanoví vážkově jako úbytek po vysušení vzorku při (103 ± 2) °C, u vlhkých nebo zvlášť vyjmenovaných krmiv po předsušení při 50 až 60 °C za předepsaných podmínek. Ve zvláštních případech se stanoví obsah vlhkosti vysušením za sníženého tlaku při 80 °C. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí pro všechny obsahy vlhkosti překročit 0,2 %. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vlhkosti: | | | do 15 % | 0,3 % | | | nad 15 % | 5 % relat. | | 1.2. | Stanovení obsahu vlhkosti a těkavých látek v tucích Účel, rozsah a princip Postup určuje podmínky pro stanovení obsahu vlhkosti a těkavých látek v tucích. Obsah vlhkosti a těkavých látek se odpaří sušením při (103 ± 2) °C a úbytek hmotnosti se stanoví vážkově. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vlhkosti: | | | do 2 % | 10 % relat. | | | nad 2 % | 0,2 % abs. | | | Reprodukovatelnost | | | Nestanovena. | | 1.3. | Stanovení obsahu vlhkosti a těkavých látek v olejnatých semenech | | | Účel, rozsah a princip | | | Postup určuje podmínky pro stanovení obsahu vlhkosti a těkavých látek v olejnatých semenech. Stanovení obsahu vlhkosti a těkavých látek se provádí buď z materiálu tak, jak byl získán (čistá semena a nečistoty) nebo, pokud je to požadováno, ze samotných čistých semen sušením při teplotě (103 ± 2) °C v sušárně při atmosférickém tlaku do konstantní hmotnosti, vážkově. | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí pro všechny obsahy vlhkosti překročit 0,2 %. | | | Reprodukovatelnost | | | Nestanovena | | 1.4. | Stanovení obsahu vlhkosti | | | Účel, rozsah princip | | | Metoda umožňuje stanovení obsahu vlhkosti v krmivech. Kromě použití pro mléčné produkty je vhodná pro většinu krmiv, minerálních surovin, krmných směsí s převážně minerální složkou a vybraných olejnatých semen a plodů. Stanovení obsahu vlhkosti olejnatých semen a plodů se řídí ustanoveními jiných právních předpisů. Obsah vlhkosti se stanoví vážkově jaro úbytek hmotnosti po vysušení vzorku krmiva za předepsaných podmínek. V případě vyššího obsahu vlhkosti krmiva je nutné předsoušení. | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí pro všechny obsahy vlhkosti překročit 0,2 %. | | | Reprodukovatelnost | | | Nestanovena. | | 1.5. | Stanovení obsahu vlhkosti v olejích a tucích | | | Účel, rozsah princip | | | Metoda umožňuje stanovení obsahu vody a těkavých látek v živočišných a rostlinných tucích a olejích. Vzorek je sušen do konstantní hmotnosti při 103 °C․ Úbytek hmotnosti je zjištěn vážením. | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí pro všechny obsahy vlhkosti překročit 0,05 %. | | | Reprodukovatelnost | | | Nestanovena. | 2. | | Dusíkaté sloučeniny | | 2.1. | Stanovení obsahu dusíkatých látek | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu dusíkatých látek v krmivech podle Kjeldahla. Postup stanovení obsahu dusíkatých látek je použitelný pro všechny obsahy ve všech druzích krmiv. Za podmínek postupu se nestanoví dusík v dusičnanech, dusitanech, popř. azo nebo hydrazosloučeninách. Po mineralizaci vzorku horkou kyselinou sírovou za přítomnosti katalyzátoru se vytěsnění amoniak hydroxidem sodným. Dusíkaté látky se stanoví titračně alkalimetricky (acidimetricky). | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu dusíkatých látek: | | | do 200 g/kg | 2 g/kg | | | od 201 g/kg do 400 g/kg | 1 % relat. | | | nad 400 g/kg | 4 g/kg | | | Reprodukovatelnost | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu dusíkatých látek | | | do 160 g/kg | 4 g/kg | | | od 160 do 320 g/kg | 2,5 % relat. | | | nad 320 g/kg | 8 g g/kg. | | 2.2. | Stanovení obsahu dusíkatých látek rozpustných působením roztoku pepsinu v kyselině chlorovodíkové | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu dusíkatých látek rozpustných působením roztoku pepsinu v kyselině chlorovodíkové v krmivech. Postup stanovení je použitelný pro všechny obsahy a všechny druhy krmiv, s výjimkou krmiv s aditivním obsahem močoviny a krmiv minerálních. Obsah dusíkatých látek rozpustných působením pepsinu v kyselině chlorovodíkové se stanoví po 48 hodinové inkubaci vzorku s pepsinem při 40 °C metodou podle Kjeldahla. | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu dusíkatých látek rozpustných působením roztoku pepsinu v kyselině chlorovodíkové: | | | do 200 g/kg | 4 g/kg | | | od 201 do 400 g/kg | 2 % relat. | | | nad 400 g/kg | 8 g/kg | | | Reprodukovatelnost | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit hodnotu 2 % relat. | | 2.3 | Stanovení obsahu bílkovin | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu bílkovin v krmivech a je použitelný pro všechna krmiva organického původu. Obsah bílkovin se stanoví metodou podle Barnsteina po jeho oddělení od dusíkatých látek nebílkovinného původu vysrážením mědnatou solí. | | | Opakovatelnost | | | Nestanovena. | | | Reprodukovatelnost | | | Nestanovena. | | 2.4 | Stanovení obsahu aminokyselin | | | Účel, rozsah princip | | | Postup specifikuje podmínky pro stanovení obsahu volných i veškerých aminokyselin v krmivech na analyzátoru aminokyselin. Metoda neumožňuje rozlišit D a L formu ani soli aminokyselin. Volné aminokyseliny se extrahují zředěnou kyselinou chlorovodíkovou. Celkový obsah aminokyselin se stanoví v oxidovaném nebo neoxidovaném vzorku po kyselé hydrolýze separací na ionexové koloně a následné reakci s ninhydrinovým činidlem fotometricky při 570 nm. Po oxidaci vzorku se stanovují aminokyseliny cystein a methionin, bez oxidace se stanovuje tyrosin a ostatní aminokyseliny (glycin, slanin, serin, threonin, valin, isoleucin, leucin, lysin, arginin, kyselina asparagová, kyselina glutamová, fenylalanin, histidin a prolin) se mohou stanovovat v oxidovaném i neoxidovaném vzorku. | | | Opakovatelnost | | | Hodnoty opakovatelnosti pro různé aminokyseliny a různá krmiva jsou součástí úplného znění metody. | | | Reprodukovatelnost | | | Hodnoty reprodukovatelnosti pro různé aminokyseliny a různá krmiva jsou součástí úplného znění metody. | | 2.5 | Stanovení obsahu močoviny | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu močoviny v krmivech s aditivním obsahem této látky. Močovina se stanoví, po vyčeření vodního výluhu vzorku Carresovými činidly, reakcí s p-dimethylaminobenzaldehydem spektofotometricky při vlnové délce 420 nm. | | | Opakovatelnost | | | Nestanovena. | | | Reprodukovatelnost | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu močoviny | | | od 2 do 20 g/kg | 2 g/kg | | | od 20 do 100 g/kg | 10 % relat. | | | od 100 do 200 g/kg | 10 g/kg | | | nad 200 g/kg | 5 % relat. | | 2.6 | Stanovení obsahu amoniaku v rybích moučkách | | | Účel; rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu amoniaku v rybích moučkách. Je použitelný pro obsahy amoniaku vyjádřené jako NH3 do hodnoty 2 500 mg/kg. Amoniak ze vzorku se extrahuje do vodního výluhu, vytěsnění se oxidem hořečnatým a stanoví se titračně alkalimetricky (acidimetricky). | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit 10% relat. | | | Reprodukovatelnost | | | Nestanovena. | | 2.7 | Stanovení obsahu těkavých dusíkatých látek | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení obsahu těkavých dusíkatých látek vyjádřených jako amoniak v krmivech. Vzorek se extrahuje vodou, těkavé dusíkaté látky se uvolní uhličitanem draselným a pomocí mikrodifuze se jímají do roztoku kyseliny borité a jsou stanoveny kyselinou sírovou titračně. | | | Opakovatelnost | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí přesáhnout při obsahu amoniaku: | | | do 10 g/kg | 10% relat. | | | rovným nebo vyšším než 10 g/kg | 1,0 g/kg | | | Reprodukovatelnost | | | Nestanovena. | | 2.8. | Stanovení aktivity ureázy v soji a jejích produktech | | | Účel, rozsah a princip | | | Postup specifikuje podmínky pro stanovení aktivity ureázy v soji a jejích produktech, do hodnoty aktivity ureázy z 1 mg N / g . min při 30 °C. Aktivita ureázy se stanoví titračně alkalimetricky určením množství amoniakálního dusíku, uvolněného z roztoku močoviny jedním gramem zkoušeného vzorku za jednu minutu při teplotě 30 °C. | | | Opakovatelnost | | | Nestanovena. | | | Reprodukovatelnost | | | Nestanovena. | | 2.9. | Ureázový test | | | Účel, rozsah a princip Postup specifikuje podmínky pro stanovení aktivity ureázy v soji a jejích produktech. Aktivita ureázy se stanoví titračně alkalimetricky určením množství amoniaku, uvolněného z roztoku močoviny ureázou ze zkoušeného vzorku za 1 hodinu. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 2.10. | Stanovení obsahu biuretu | | | Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu biuretu v močovině. Postup je založen na tvorbě barevného komplexu biuretu se síranem měďnatým a měření absorbance vybarveného roztoku při vlnové délce 540 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit 0,3 g/kg. Reprodukovatelnost Nestanovena. | | 2.11. | Stanovení obsahu hydroxyanalogu methioninu | | | Účel, rozsah a princip Obsah hydroxyanalogu methioninu se stanoví po extrakci vzorku směsí voda-acetonitril a následné hydrolýze metodou HPLC na reverzní fázi s použitím UV detekce. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 2.12. | Stanovení obsahu dusíkatých látek rozpustných působením pepsinu Účel, rozsah a princip Metoda je použitelná pro stanovení podílu dusíkatých látek rozpustných působením pepsinu a kyseliny chlorovodíkové za definovaných podmínek. Vzorek krmiva v roztoku pepsinhydrochloridu je zahříván po dobu 48 hodin na teplotu 40 °C. Suspense je zfiltrována a ve filtrátu je stanoven obsah dusíkatých látek metodou 2.1. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro obsahu dusíkatých látek rozpustných působením pepsinu: | | | do 200 g/kg | 4 g/kg | | | od 200 do 400 g/kg | 2 % relat. | | | nad 400 g/kg | 8 g/kg | | | Reprodukovatelnost Nestanovena. | | 2.13. | Stanovení aktivity pepsinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení aktivity pepsinu, který se používá k určení obsahu dusíkatých látek rozpustných působením roztoku pepsinu v kyselině chlorovodíkové. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 2.14. | Stanovení obsahu methioninu Účel, rozsah a princip Obsah methioninu v premixech se stanoví po extrakci vzorku fosfátovým pufrem a následné reakci s jodem za vzniku komplexu methionin - jod při pH 6,5. Komplex se reverzibilně rozkládá při pH 1 zpět na jod a methionin. Uvolněný jod se stanoví titračně jodometricky. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 2.15. | Stanovení obsahu tryptofanu Účel, rozsah a princip Tryptofan se stanoví po alkalické hydrolýze hydroxidem lithným metodou vysokoúčinné kapalinové chromatografie na reverzní fází s fluorescenční detekcí (excitační vlnová délka 283 nm, emisní vlnová délka 355 nm). Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | 3. | | Tuk | | 3:1. | Stanovení obsahu tuku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu tuku (hexanového, petroletherového nebo diethyletherového extraktu) v krmivech. Postup není vhodný pro stanovení obsahu tuku v olejninách. Tuk ze vzorku se izoluje buď přímou extrakcí příslušným extrakčním činidlem, nebo extrakcí po předběžné hydrolýze a obsah tuku se stanoví vážkově. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro obsah tuku: | | | do 50 g/kg | 2 g/kg | | | od 51 do 100 g/kg | 4 % relat. | | | nad 100 g/kg | 4 g/kg | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu tuku: | | | od 4 do 100 g/kg | 4 g/kg | | | od 100 do 200 g/kg | 4 % relat. | | | nad 200 g/kg | 8 g/kg | | 3.2. | Stanovení obsahu tuku v olejnatých semenech Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu tuku (hexanového nebo petroletherového extraktu) v olejnatých semenech. Obsah tuku („oleje”) se stanoví po extrakci vzorku hexanem nebo petroletherem na vhodném zařízení, následným oddestilováním extrakčního činidla a zvážením vysušeného vyextrahovaného tuku. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit hodnotu 4 g/kg. Reprodukovatelnost Nestanovena. | | 3.3. | Stanovení čísla kyselosti tuku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení čísla kyselosti tuku v krmivech. Číslo kyselosti tuku se stanoví titračně alkalimetricky, po rozpuštění tuku vyextrahovaného z krmiva ve směsi extrakční činidlo - ethylalkohol. Způsob extrakce tuku závisí na druhu zkoušeného krmiva. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku pro hodnoty větší než 4 mg KOH/g (resp. 0,07 mmol/g) nesmí překročit 5% relativních. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí při hodnotě nad 4 mg KOH/g tuku překročit hodnotu 15 % relat. | | 3.4. | Stanovení obsahu lecitinu Účel, rozsah a princip Postup je určen ke stanovení obsahu lecitinu v technických a potravinářských produktech. Stanoví se obsah látek rozpustných v acetonu, obsah látek nerozpustných v benzenu nebo toluenu a obsah vody s těkavými látkami a jejich součet se odečte od 100. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit 10 g/kg. Reprodukovatelnost Nestanovena. | | 3.5. | Stanovení obsahu nerozpustných nečistot v tucích a olejích Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu nerozpustných nečistot v živočišných a rostlinných tucích nebo olejích. Obsah nerozpustných nečistot se stanoví rozpuštěním vzorku v přebytku a-hexanu nebo petroletheru nebo diethyletheru, filtrací získaného roztoku a zvážením vysušeného filtru s nerozpustnými nečistotami. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu nerozpustných nečistot: | | | do 3,0 g/kg | 0,2 g/kg | | | nad 3,0 g/kg | 0,5 g/kg | | | Reprodukovatelnost Nestanovena. | | 3.6. | Stanovení obsahu nezmýdelnitelných látek v tucích a olejích Účel; rozsah a princip Postup specifikuje podmínky pro stanovení nezmýdelnitelného podílu v živočišných a rostlinných tucích a olejích. Postup není použitelný pro vosky a dává přibližné výsledky u určitých tuků s vyšším obsahem nezmýdelnitelného podílu, např. u tuků pocházející z mořských živočichů. Tuk nebo olej se zmýdelní varem s ethanolickým roztokem hydroxidu draselného pod zpětným chladičem. Nezmýdelnitelný podíl se vyextrahuje z roztoku mýdla diethyletherem a po oddestilování rozpouštědla a vysušení se zváží. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu nezmýdelnitelných látek: | | | do 50 g/kg | 0,5 g/kg | | | od 50 do 100 g/kg | 1 g/kg. | | | Reprodukovatelnost Nestanovena. | | 3.7. | Stanovení peroxidového čísla Účel, rozsah a princip Postup specifikuje podmínky pro stanovení peroxidového čísla v živočišných a rostlinných tucích a olejích. Peroxidové číslo se určí reakcí chloroformového extraktu vzorku s jodidem draselným v roztoku kyseliny octové a chloroformu a následnou titrací uvolněného jodu odměrným roztokem thiosíranu sodného. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí přesáhnout při hodnotě peroxidového čísla: | | | méně než 0,5 mmol/kg | 0,1 mmol/kg | | | od 0,5 do 3 mmol/kg | 0,2 mmol/kg | | | od 3 do 6 mmol/kg | 0,5 mmol/kg | | | větší než 6 mmol/kg | 1,0 mmol/kg | | | Reprodukovatelnost Nestanovena. | | 3.8. | Stanovení obsahu oleje a tuku Účel, rozsah a princip Metoda umožňuje stanovení obsahu oleje a tuku v krmivech. Stanovení obsahu oleje a tuku olejnatých semen a plodů se řídí ustanoveními jiných právních předpisů. Podle druhu krmiva se používají dvě modifikace postupu. Metoda A vhodná pro všechny krmiva kromě krmiv uvedených v metodě B. Metoda B použitelná pro krmiva obsahující tuk a olej, který nemůže být kvantitativně extrahován petroletherem bez předchozí hydrolýzy, jako gluten, kvasnice, sojové a bramborové proteiny. Metoda je dále použitelná pro krmné směsi obsahující sušené mléko. Metoda A - tuk a olej je extrahován petroletherem a po jeho oddestilování je vysušen a zvážen. Metoda B - vzorek je hydrolyzován horkou kyselinou chlorovodíkovou a zbytek po promytí a vysušení je extrahován petroletherem podle metody A. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu tuku: | | | do 50 g/kg | 2 g/kg | | | od 50 do 100 g/kg | 4 % relat. | | | nad 100 g/kg | 4 g/kg | | | Reprodukovatelnost Nestanovena. | 4. | | Polysacharidy | | „4.1. | Stanovení obsahu vlákniny Účel, rozsah a princip . Používají se dvě modifikace postupu, pro manuální a přístrojové provedení. Obsah vlákniny se stanoví vážkově jako nezhydrolyzovatelný zbytek vzorku po kyselé a alkalické hydrolýze, od kterého se odečte obsah popele. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro obsahu vlákniny: | | | do 100 g/kg | 3 g/kg | | | nad 100 g/kg | 3 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vlákniny: | | | od 4 do 100 g/kg | 4 g/kg | | | nad 100 g/kg | 4 % relat. | 5. | | Bezdusíkaté látky výtažkové | | | 5.1. Stanovení obsahu škrobu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení celkového obsahu škrobu v krmivech. Postup nelze použít pro krmiva s relativně vysokým obsahem polymerů fruktosy, konkrétně pro krmiva, obsahující řepné řízky a bulvy, skrojky, jakož i zdrtky těchto plodin, kvasnice a krmiva bohatá na inulin. Škrob se stanoví polarimetricky po hydrolýze vzorku kyselinou chlorovodíkovou a odstranění bílkovin Carresovými činidly, změřením optické otáčivosti a provedením korekce na opticky aktivní látky rozpustné ve směsi ethylalkohol-voda. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro obsahy škrobu : | | | nižší než 400 g/kg | 4 g/kg | | | vyšší než 400 g/kg | 1 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu škrobu: | | | do 120 g/kg | 6 g/kg | | | od 120 do 200 g/kg | 5 % relat. | | | nad 200 g/kg | 10 g/kg | | 5.2. | Stanovení obsahu škrobu - pankreaticky postup Účel, rozsah a princip Postup specifikuje podmínky pro stanovení škrobu a výše molekulárních degradačních produktů škrobu v krmivech obsahujících řepné řízky, skrojky, rajčatovou pastu, sušené kvasnice a krmiva bohatá na inulin. Stanovení škrobu v těchto materiálech se provádí pouze tehdy, jestliže mikroskopické vyšetření prokáže přítomnost dostatečného množství škrobu. Cukry přítomné ve vzorku se extrahují ethanolem. Škrob v extrakčním zbytku se rozloží pankreatinem, vzniklé cukry se hydrolyzují kyselinou chlorovodíkovou a vzniklá glukosa se stanoví Luff-Schoorlovou metodou. Obsah škrobu se zjistí vynásobením množství glukosy konstantním faktorem. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 5.3. | Stanovení obsahu cukrů Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu cukrů v krmivech a je použitelný pro všechna krmiva včetně krmných směsí a pro všechny obsahy cukrů. Obsah cukrů se stanoví v ethylalkoholickém extraktu vzorku titračně jodometricky postupem podle Luff-Schoorla. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro obsahu cukrů: | | | od 15 do 100 g/kg | 3 g/kg | | | nad 100 g/kg | 3 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu cukrů: | | | od 5 do 250 g/kg | 5 g/kg | | | od 250 do 500 g/kg | 2 % relat. | | | Nad 500 g/kg | 10 g/kg | | 5.4. | Stanovení obsahu laktosy Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu laktosy v krmivech. Postup je použitelný pro krmiva obsahující více než 5 g laktosy v 1 kg krmiva. Laktosa se spolu s ostatními cukry se vyextrahuje ze vzorku vodou, extrakt se vystaví fermentačnímu účinku kvasinek Saccharomyces cerevisiae, které ponechají laktosu v nezměněném stavu. Po vyčeření Carresovými činidly se laktosa stanoví titračně jodometricky podle Luff-Schoorla. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 5.5. | Stanovení obsahu bezdusíkatých látek výtažkových výpočtem Účel, rozsah a princip Postup uvádí způsob výpočtu obsahu bezdusíkatých látek výtažkových z výsledků stanovení základních složek krmiv a to vlhkosti, dusíkatých látek (N x 6,25), tuku, popele a vlákniny případně močoviny a amoniaku. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 5.6. | Stanovení obsahu cukrů polarizací Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu cukrů polarizací v krmném cukru, melase a mléce. Pro stanovení obsahu cukrů se využívá jejich schopnosti otáčet rovinu polarizovaného světla úměrně druhu a obsahu cukru v roztoku. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku pro všechny obsahy cukrů nesmí překročit 1 g/kg. Reprodukovatelnost Nestanovena. | | 5.7. | Stanovení obsahu redukujících látek v cukru a melase Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu redukujících látek v surovém a afinovaném cukru a řepné melase. Cukerný roztok se povaří s Ofnerovým roztokem a vyloučený oxid měďný se stanoví jodometrickou titrací. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | 6. | | Popel | | 6.1. | Stanovení obsahu popele Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu popele v krmivech. Postup je použitelný pro všechna krmiva obsahující výhradně či převážně organickou složku a pro všechny obsahy popele. Obsah popele se stanoví vážkově jako zbytek hmoty po zpopelnění při teplotě 550 °C do konstantní hmotnosti za předepsaných podmínek. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu popele: | | | do 30 g/kg | 3 g/kg | | | od 31 do 50 g/kg | 10 relat. | | | od 51 do 200 g/kg | 5 g/kg | | | od 201 do 400 g/kg | 2,5 % telat. | | | nad 400 g/kg | 10 g/kg | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu popele : | | | od 2 do 40 g/kg | 10 % relat. | | | od 40 do 100 g/kg | 4 g/kg | | | od 100 do 150 g/kg | 4 %relat. | | | od 150 do 200 g/kg | 6 g/kg | | | nad 200 g/kg | 3 % telat. | | 6.2. | Stanovení obsahu popele v tucích Účel, rozsah a princip Postup specifikuje podmínky pro stanovení popele a je použitelný pro všechny živočišné a rostlinné tuky a oleje včetně kyselých tuků. Obsah popele je anorganický zbytek po zpopelnění za stanovených podmínek. Vzorek tuku se spálí při určené teplotě a získaný zbytek se určí vážkově. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu popele v tucích: | | | do 1 g/kg | 20% relat. | | | nad 1 g/kg | 15% relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu popele v tucích: | | | do 1,6 g/kg | 0,2 g/kg | | | od 1,6 do 80 g/kg | 12,5 % relat. | | | nad 80 g/kg | 10 g/kg | | 6.3. | Stanovení obsahu nerozpustného podílu popele v kyselině chlorovodíkové Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu nerozpustného podílu popele v kyselině chlorovodíkové v krmivech a premixech.. Postup je použitelný pro všechny obsahy nerozpustného podílu popele v kyselině chlorovodíkové. Podíl popele nerozpustného v kyselině chlorovodíkové se stanoví vážkově jako zbytek po rozpuštění popele, resp. přímým rozpuštění vzorku, v kyselině chlorovodíkové. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu nerozpustného podílu popele v kyselině chlorovodíkové: | | | do 10 g/kg | 1 g/kg | | | od 11 do 50 g/kg | 10 %-relat. | | | od 51 do 200 g/kg | 5 g/kg | | | od 201 do 400 g/kg | 2,5 % relat. | | | nad 400 g/kg | 10 g/kg | | | Reprodukovatelnost. Nestanovena. | | 6.4. | Stanovení obsahu popele nerozpustného v kyselině chlorovodíkové Účel, rozsah a princip Metoda umožňuje stanovení obsahu minerálních látek, nerozpustných v kyselině chlorovodíkové v krmivech. Podle původu vzorku mohou být použity dvě různé metody. Metoda A: použitelná pro organická krmiva a pro většinu krmných směsí. Vzorek se zpopelní, popel se povaří s kyselinou chlorovodíkovou a nerozpuštěný zbytek se zfiltruje a zváží. Metoda B: použitelná pro minerální suroviny nebo minerální doplňková krmiva a krmné směsi s obsahem látek nerozpustných v kyselině chlorovodíkové, stanovených metodou A, vyšší než 10 g/kg. Vzorek se rozpouští v kyselině chlorovodíkové. Roztok se zfiltruje, zbytek na filtru se zpopelní a dále se postupuje podle metody A. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | 7. | | Makroprvky | | 7.1. | Stanovení obsahu fosforu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu fosforu v krmivech a premixech. Obsah fosforu se stanoví po reakci s molybdátovanadátovým činidlem spektrofotometricky nebo po vysrážení chinolinovým činidlem vážkově nebo metodou atomové emisní spektrometrie v indukčně vázaném plazmatu (ICP). Opakovatelnost Rozdíl mezi dvěma paralelními spektrofotometrickými stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu fosforu: | | | do 50 g/kg | 3 % relat. | | | nad 50 g/kg | 1,5 g/kg | | | Opakovatelnost pro postup vážkový a pro metodu ICP nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky vážkových a spektrofotometrických zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu fosforu: | | | do 10 g/kg | 0,6 g/kg | | | nad 10 g/kg | 6 % relat. | | | Reprodukovatelnost pro postup spektrometrický (ICP) nestanovena. | | 7.2. | Stanovení obsahu vápníku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vápníku v krmivech a premixech od obsahu 0,5 g/kg. Obsah vápníku se stanoví z chloridového výluhu popele vzorku. Stanoví se titračně manganometricky nebo vážkově jako síran vápenatý nebo metodou atomové absorpční spektrometrie (AAS) nebo metodou atomové emisní spektrometrie v indukčně vázaném plazmatu (ICP) nebo titračně chelatometricky (pro krmné směsi). Opakovatelnost Rozdíl mezi dvěma paralelními manganometrickými stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vápníku: | | | pod 50 g/kg | 1 g/kg | | | nad 50 g/kg | 2 % relat. | | | Rozdíl mezi dvěma paralelními chelatometrickými stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vápníku: | | | do 10 g/kg | 0,4 g/kg | | | od 10 do 100 g/kg | 4 % relat. | | | nad 100 g/kg | 4 g/kg | | | Opakovatelnost pro postup vážkový a spektrometrický (AAS, ICP) nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky manganometrických a chelatometrických zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vápníku: | | | od 1 do 5 g/kg | 0,5 g/kg | | | od 5 do 60 g/kg | 10 % relat. | | | od 60 do 100 g/kg | 6 g/kg | | | nad 100 g/kg | 6 % relat. | | | Reprodukovatelnost pro postup vážkový a spektrometrický (AAS, ICP) nestanovena. | | 7.3. | Stanovení obsahu hořčíku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu celkového hořčíku v krmivech a premixech. Postup je vhodný zejména pro obsahy do 50 g/kg. Obsah hořčíku se stanoví po mineralizaci vzorku v chloridovém výluhu metodou atomové absorpční spektrometrie (AAS) nebo metodou atomové emisní spektrometrie v indukčně vázaném plazmatu (ICP). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro všechny obsahy hořčíku 5 % relat. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu hořčíku: | | | od 2 do 50 g/kg | 10 % relat. | | | nad 50 g/kg | 5 g/kg | | 7:4. | Stanovení obsahu draslíku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení celkového obsahu draslíku v krmivech a premixech. Obsah draslíku se stanoví v chloridovém výluhu po zpopelnění vzorku metodou emisní plamenové spektrometrie. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu draslíku: | | | od 2 do 50 g/kg | 10 % relat. | | | nad 50 g/kg | 5 g/kg | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu draslíku: | | | od 2 do 50 g/kg | 10 % relat. | | | nad 50 g/kg | 5 g/kg | | 7.5. | Stanovení obsahu sodíku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení celkového obsahu sodíku v krmivech a premixech. Obsah sodíku se stanoví v chloridovém výluhu po zpopelnění vzorku metodou emisní plamenové spektrometrie. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu sodíku | | | od 2 do 50 g/kg | 10 % relat. | | | nad 50 g/kg | 5 g/kg | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu sodíku: | | | od 0,4 do 1,6 g/kg | 0,2 g/kg | | | od 1,6 do 80 g/kg | 12,5 % relat. | | | nad 80 g/kg | 10 g/kg | | 7.6. | Stanovení obsahu ve vodě rozpustných chloridů Účel, rozsah a princip Postup specifikuje podmínky pro stanovení ve vodě rozpustných chloridů v krmivech a premixech. Postup včetně modifikací zahrnuje použití pro všechna krmiva a všechny obsahy ve vodě rozpustných chloridů. Chloridy se stanoví nepřímou argentometrickou titrací podle Volharda z vodního výluhu vzorku po vyčeření Carresovými činidly. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu chloridů: | | | do 10 g/kg | 0,5 g/kg | | | nad 10 g/kg | 5 % relat. | | | (rybí moučky | 10 % relat.) | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit pro všechny obsahy ve vodě rozpustných chloridů hodnotu 20 % relat. | | 7.7. | Stanovení obsahu celkových uhličitanů Postup specifikuje podmínky pro stanovení celkových uhličitanů v krmných směsích a je použitelný pro obsahy od 5 do 100 g/kg. Obsah celkových uhličitanů se stanoví po rozkladu vzorku kyselinou chlorovodíkovou a vzniklý oxid uhličitý se změří v kalibrované trubici volumetricky nebo manometricky. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu celkových uhličitanů: | | | od 5 do 25 g/kg | 2 g/kg | | | od 25 do 100 g/kg | 8 % relat. | | | nad 100 g/kg | 8 g/kg. | | 7.8. | Stanovení obsahu oxidů křemíku, hliníku, vápníku a hořčíku (ve vápencích) Účel, rozsah a princip Postup specifikuje podmínky pro stanovení uvedených oxidů ve vápencích. Po rozkladu vzorku tavením se stanoví obsah oxidu křemičitého vážkově. Ve filtrátu po stanovení oxidu křemičitého se stanoví oxid železitý a hlinitý vážkově. Ve filtrátu po stanovení oxidu železitého a hlinitého se stanoví oxid vápenatý a hořečnatý titračně chelatometricky. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními obsahu oxidu křemičitého prováděnými na stejném vzorku nesmí překročit 2 g/kg. Rozdíl mezi dvěma paralelními stanoveními obsahu oxidů amoniakální skupiny prováděnými na stejném vzorku nesmí překročit při obsahu oxidů amoniakální skupiny: | | | do 10 g/kg | 0,7 g/kg | | | od 10,1 do 25 g/kg | 1,0 g/kg | | | od 25,1 do 50 g/kg | 1,5 g/kg | | | od 50,1 do 100 g/kg | 2,5 g/kg | | | nad 100 g/kg | 4,0 g/kg | | | Rozdíl mezi dvěma paralelními stanoveními obsahu oxidu vápenatého prováděnými na stejném vzorku nesmí překročit 4,5 g/kg. Rozdíl mezi dvěma paralelními stanoveními obsahu oxidu hořečnatého prováděnými na stejném vzorku nesmí překročit při obsahu: | | | do 10 g/kg | 1,5 g/kg | | | nad 10 g/kg | 3 g/kg | | | Reprodukovatelnost Nestanovena. | | 7.9. | Stanovení celkového obsahu síry Účel, rozsah a princip Postup specifikuje podmínky pro stanovení celkového obsahu síry v krmivech. Je vhodný pro všechny obsahy síry v krmivech. Obsah síry se stanoví v chloridovém výluhu po zpopelnění vzorku vážkově jako síran barnatý. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 7.10. | Stanovení obsahu vápníku Účel, rozsah a princip Metoda umožňuje stanovení obsahu celkového vápníku v krmivech. Vzorek se zpopelní, popel se rozpustí v kyselině chlorovodíkové a vápník se vysráží jako šťavelan vápenatý. Sraženina se rozpustí v kyselině sírové a uvolněná kyselina šťavelová se titruje manganistanem draselným. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | 8. | | Mikroprvky | | 8.1. | Stanovení obsahů mědi, železa, manganu a zinku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení mědi, železa, manganu a zinku v krmivech a premixech. Uvedenými postupy lze stanovit všechny formy uvedených prvků. Obsah mědi, železa, manganu a zinku se stanoví po mineralizaci vzorku v chloridovém výluhu metodou atomové absorpční spektrometrie (AAS) nebo metodou atomové emisní spektrometrie v indukčně vázaném plazmatu (ICP). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu mědi, železa, manganu a zinku: | | | do 50 mg/kg | 5 mg/kg | | | od 50 do 100 mg/kg | 10 % relat. | | | od 100 do 200 mg/kg | 10 mg/kg | | | nad 200 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. | | 8.2. | Stanovení obsahu manganu, zinku, mědi, železa, hořčíku, draslíku, sodíku a vápníku Účel, rozsah a princip Postup specifikuje stanovení obsahu mikroprvků manganu, zinku, mědi, železa a makroprvků hořčíku, draslíku, sodíku a vápníku v krmivech a premixech. Vzorek se převede do roztoku kyselinou chlorovodíkovou, pokud je třeba po zpopelnění, případně po odstranění kysličníku křemičitého a uvedené prvky se stanoví po vhodném naředění metodou atomové absorpční spektrometrie (AAS). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit hodnotu pro stanovení obsahu vápníku, železa, draslíku, hořčíku a manganu 0,11 . X mg/kg a pro stanovení obsahu mědi, sodíku a zinku 0,15 . X mg/kg kde X je výsledek stanovení. Uvedená opakovatelnost platí pro obsahy: | | | vápníku | od 1 000 do 300 000 mg/kg | | | mědi | od 15 do 15 000 mg/kg | | | železa | od 2 000 do 30 000 mg/kg | | | hořčíku | od 1 000 do 110 000 mg/kg | | | manganu | od 15 do 15 000 mg/kg | | | sodíku | od 2 000 do 250 000 mg/kg | | | zinku | od 25 do 15 000 mg/kg | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu mědi, železa, manganu, zinku, hořčíku, draslíku, sodíku a vápníku: | | | do 5 mg/kg | 50 % relat. | | | od 5 do 10 mg/kg | 2,5 mg/kg | | | od 10 do 30 mg/kg | 25 % relat. | | | od 30 do 50 mg/kg | 7,5 mg/kg | | | nad 50 mg/kg | 15 % relat. | | 8.3. | Stanovení obsahů mědi, železa, manganu a zinku Účel, rozsah a princip Postup specifikuje podmínky pro stanoveni mědi, železa, manganu a zinku v krmivech a premixech. Uvedenými postupy lze stanovit všechny formy uvedených prvků. Obsah mědi, železa, manganu a zinku se stanoví po mineralizaci vzorku v chloridovém výluhu metodou atomové absorpční spektrometrie (AAS). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu mědi, železa, manganu a zinku: | | | do 50 mg/kg | 5 mg/kg | | | od 50 do 100 mg/kg | 10 % relat. | | | od 100 do 200 mg/kg | 10 mg/kg | | | nad 200 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti pro stanovení železa je 20 mg/kg, pro stanovení mědi je 10 mg/kg, pro stanovení manganu je 20 mg/kg, pro stanovení zinku je 20 mg/kg. | 9. | | Kyselost | | 9.1. | Stanovené volné, vázané a celkové kyselosti vodního výluhu Účel, rozsah a princip . Postup specifikuje podmínky pro stanovení volné, vázané i celkové kyselosti vodního výluhu. Je použitelný pro všechna krmiva. Volná kyselost vodního výluhu se stanoví přímo alkalimetrickou titrací vodního výluhu vzorku do hodnoty pH = 8,5 nebo na indikátor fenolftalein. Vázaná kyselost vodního výluhu se stanoví po uvolnění vazeb vnitřní neutralizace formaldehydem alkalimetrickou titrací do hodnoty pH = 8,5 nebo na indikátor fenolftalein. Celková kyselost vodního výluhu se určí součtem výsledků volné a vázané kyselosti vodního výluhu. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit pro všechny hodnoty kyselosti 15 % relat. Reprodukovatelnost Nestanovena. | | 9.2. | Stanovení kyselosti vodního výluhu v mléčných krmných směsích Účel, rozsah a princip Postup specifikuje podmínky pro stanovení kyselosti vodního výluhu v mléčných krmných směsích. Je použitelný pro všechny druhy mléčných krmných směsí a všechny obsahy kyselosti. Kyselost vodního výluhu se stanoví ve vodním výluhu vzorku přímo alkalimetrickou titrací na indikátor fenolftalein pomocí určení bodu ekvivalence srovnávacím roztokem kobaltnaté soli. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | 10. | | Nežádoucí látky | | 10.1. | Stanovení obsahu kyanovodíku Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu kyanovodíku volného i vázaného v glukosinolátech v krmivech, zejména v lněném semeni, maniokové mouce a v některých druzích bobů. Vzorek se rozmíchá ve vodě, kyanovodík se uvolní enzymaticky a vodní parou se předestiluje do okyseleného roztoku dusičnanu stříbrného. Kyanid stříbrný se oddělí filtrací a zbylý dusičnan stříbrný se stanoví titračně thiokyanatanem amonným. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 10.2. | Stanovení obsahu hořčičného oleje vyjádřeného jako allylisothiokyanátu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu hořčičného oleje ve výliscích rodu Brassica a Sinapis a v krmných směsích, které tyto šroty obsahují. Hořčičný olej se vyjadřuje jako allylisothiokyanát. Hořčičný olej se enzymaticky uvolní, vytěsní destilací a po reakci s dusičnanem stříbrným se stanoví obsahu allylisothiokyanátu titračně. Opakovatelnost Nestanovena Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí pro všechny obsahy hořčičného oleje překročit 20 % relat. | | 10.3. | Stanovení obsahu theobrominu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu theobrominu v krmivech a premixech Obsah theobrominu se stanoví po extrakci ze vzorku směsným rozpouštědlem chloroform-amoniak metodou vysokoúčinné kapalinové chromatografie (HPLC) na reversní fázi. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 10.4. | Stanovení obsahu glukosinolátů v řepce Účel, rozsah a princip Postup specifikuje podmínky pro stanovení nejdůležitějších glukosinolátů v řepce a jejích produktech. Obsah glukosinulátů se stanoví po enzymatické hydrolýze v prostředí pufru metodou plynové chromatografie. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena: | | 10.5. | Stanovení obsahu 5-vinyl-2-thiooxazolidonu (goitrinu) Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vinylthiooxazolidonu (VOT) v krmivech a je použitelný pro obsahy od 200 mg/kg. Ze vzorku krmiva je enzymaticky uvolněn 2-hydroxy-3-butenyl-isothiokyanát, ze kterého vzniká VOT a jeho obsah se stanoví metodou plynové chromotografie (GC) nebo vysokoúčinné kapalinové chromatografie (HPLC). Opakovatelnost Nestanovena Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí pro všechny obsahy 5-vinyl-2-thiooxazolidonu překročit 20 % relat. | | 10:6. | Stanovení obsahu kyseliny erukové Účel, rozsah a princip Postup specifikuje podmínky pro stanovení kyseliny erukové ve všech druzích rostlinných tuků a olejů různého stupně čištění. Obsah kyseliny erukové ( kyselin cis, trans-11 dokosenové a cis,trans 13-dokosenové) je vyjádřen jako hmotnostní podíl mastných kyselin C 22 : 1 z celého spektra mastných kyselin ve vzorku. Obsah kyseliny erukové se stanoví po esterifikaci mastných kyselin metodou plynové chromatografie. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 10.7. | Stanovení obsahu olova a kadmia Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu olova a kadmia v krmivech. Postup není vhodný pro premixy. Obsah olova a kadmia se stanoví v dusičnanovém výluhu popele metodou plamenové atomové absorpční spektrometrie (AAS) nebo anodické rozpouštěcí voltametrie s předkoncentrací na visící rtuťové kapkové elektrodě. Opakovatelnost Nestanovena Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu olova: | | | od 1 do 3 mg/kg | 50 % relat. | | | od 3 do 5 mg/kg | 1,5 mg/kg | | | od 5 do 10 mg/kg | 30 % relat. | | | od 10 do 20 mg/kg | 3 mg/kg | | | od 20 do 40 mg/kg | 15 % relat. | | | od 40 do 60 mg/kg | 6 mg/kg | | | nad 60 mg/kg | 10 % relat. | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu kadmia: | | | od 0,1 do 0,2 mg/kg | 50 % relat. | | | od 0,2 do 0,4 mg/kg | 0,1 mg/kg | | | od 0,4 do 1 mg/kg | 25 % relat. | | | od 1 do 2,5 mg/kg | 0,25 mg/kg | | | nad 2,5 mg/kg | 10 % relat. | | 10.8. | Stanovení obsahu ricinových slupek Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu ricinových slupek v krmivech a zejména v olejnatých semenech. Ricinové slupky se uvolní vyvařením zkušebního vzorku v kyselém a alkalickém prostředí a jejich obsah se stanoví vážkově. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. | | 10.9. | Stanovení obsahu fluoru Účel, rozsah a princip Postup specifikuje podmínky pro stanovení fluoru v krmivech. Obsah fluoru se stanoví v chloridovém výluhu popele iontově selektivní elektrodou. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu fluoru: | | | do 12 mg/kg | 50 % relat. | | | od 12 do 15 mg/kg | 6 mg/kg | | | od 15 do 30 mg/kg | 40 % relat. | | | od 30 do 60 mg/kg | 12 mg/kg | | | od 60 do 500 mg/kg | 20 % relat. | | | od 500 do 1000 mg/kg | 100 mg/kg | | | nad 1000 mg/kg | 10 % relat. | | 10.10. | Stanovení obsahu reziduí organochlorových a organofosfátových pesticidů Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu aldrinu, dieldrinu, DDT, DDE, TDE, endrinu, heptachloru, hexachlorcyklohexanu (HCH) a polychlorované bifenyly (PCB) v krmivech. Residua pesticidů a polychlorovaných bifenylů (PCB) se extrahují z krmiv vhodným rozpouštědlem a v extraktu se stanoví jejich obsah pomocí chromatografických metod (papírové, tenkovrstevné nebo plynové). Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 10.11. | Stanovení obsahu hexachlorbenzenu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení hexachlorbenzenu (HCB) v tucích. Hexachlorbenzen (HCB) se stanoví po přečištění a extrakci metodou plynové chromatografie. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 10.12. | Stanovení obsahu dusitanů Účel , rozsah a princip Postup specifikuje podmínky pro stanovení dusitanů v krmivech. Ve filtrátu alkalického výluhu vzorku se obsah dusitanů stanoví po diazotaci kyselinou sulfanilovou a následné kopulaci s N-naftyl-1-etylendiamin dihydrochloridem spektrofotometricky. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 10.13. | Stanovení obsahu rtuti Účel, rozsah a princip Postup specifikuje podmínky pro stanovení rtuti v krmivech. Rtuť v krmivech se stanoví metodou studených par na rtuťovém analyzátoru TMA (AMA). Opakovatelnost Nestanovena Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu rtuti: | | | od 0,04 do 0,06 mg/kg | 50 % relat. | | | od 0,06 do 0,1 mg/kg | 0,03 mg/kg | | | od 0,1 do 0,2 mg/kg | 30 % relat. | | | od 0,2 do 0,3 mg/kg | 0,06 mg/kg | | | nad 0,3 mg/kg | 20 % relat. | | 10.14. | Stanovení obsahu aflatoxinu B1 Účel, rozsah a princip Postup specifikuje podmínky pro stanovení aflatoxinu B1 v krmivech; včetně těch, která obsahují slupky citrusů. Vzorek krmiva se extrahuje chloroformem, získaný extrakt se zfiltruje a přečistí na pevné fázi. Konečné rozdělení a stanovení se provede technikou vysokoúčinné kapalinové chromatografie (HPLC), za použití reverzní fáze a postkolonové derivatizace jodem a fluorescenční detekce. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu aflatoxinu B1: | | | do 20 µg/kg | 25 % relat. | | | od 20 µg/kg do 50 µg/kg | 5 µg/kg | | | nad 50 µg/kg | 10 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu aflatoxinu B1: | | | do 20 µg/kg | 50 % relat. | | | od 20 µg/kg do 50 µg/kg | 10 µg/kg | | | nad 50 µg/kg | 20 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 1 µg/kg. | | 10.15. | Stanovení obsahu arsenu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení arsenu v krmivech. Ve vzorku se po rozkladu kyselinou dusičnou v uzavřeném systému stanoví obsah arsenu metodou atomové absopční spektrometrie (AAS) s hydridovou technikou. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu arsenu: | | | do 1 mg/kg | 50 % relat. | | | od 1 do 2,5 mg/kg | 0,5 mg/kg | | | od 2,5 do 15 mg/kg | 20 % relat. | | | od 15 do 30 mg/kg | 3 mg/kg | | | nad 30 mg/kg | 10 % relat.”. | | 10.16. | Stanovení obsahu gossypolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu volného a celkového gossypolu a chemicky příbuzných látek v koncentraci nad 20 mg/kg v bavlníku a krmných směsích, které bavlník obsahují. Gossypol se extrahuje buď za přítomnosti 3-amino-1-propanolu (při stanovení volného gossypolu) nebo dimethylfbrmamidu (při stanovení celkového gossypolu). Gossypol je reakcí s anilinem převeden na gossypol-dianilid a absorbance roztoku je měřena při 440 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 10.17. | Stanovení obsahu theobrominu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení theobrominu v krmivech. Obsah theobrominu se stanoví po extrakci vzorku směsným rozpouštědlem chloroform - amoniak metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti nestanovena. | 11. | | Zkoušení siláží | | 11.1. | Zkoušení jakosti siláží Účel, rozsah a princip Postup specifikuje podmínky pro zkoušení jakosti konzervace silážovaných krmiv. Uvedené postupy zkoušení jsou použitelné pro všechny druhy silážovaných krmiv. Ze vzorku siláže se připraví vodní výluh. Ve ,výluhu se určí hodnota pH elektrometricky, obsah amoniaku se stanoví difuzní Conwayovou metodou, obsah alkoholu se stanoví metodou plynové chromatografie a obsah silážních kyselin metodou kapilární izotachoforézy. Stanovení stlačitelnosti u řízkových siláží se provádí z upraveného vzorku. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit: | | | u stanovení pH | 0,05 | | | formolové titrace | 0,1 g/kg | | | obsahu amoniaku jako NH3 | 0,1 g/kg | | | obsahu silážních kyselin | 1,0 g/kg | | | U stanovení obsahu alkoholu a stlačitelnosti siláží nebyla opakovatelnost zatím stanovena. Reprodukovatelnost Nestanovena.”. |
|
| 29. | Příloha č. 10 zní „Příloha č. 10 k vyhlášce č. 222 /1996 Sb. Postupy prolaboratorní zkoušení krmiv, doplňkových látek a premixů Seznam postupů chemického zkoušení doplňkových látek, premixů a krmných směsí s doplňkovými látkami a premixy Název postupu | Označení postupu | 1. | Stimulátory růstu | | 1.1. | Stanovení obsahu avilamycinu | -A- | 1.2. | Stanovení obsahu avoparcinu | -A- | 1.3. | Stanovení obsahu flavosfolipolu | -A- | 1.4. | Stanovení obsahu olachindoxu | -B- | 1.5. | Stanovení obsahu monensinu | -A- | 1.6. | Stanovení obsahu monensinu | -A- | 1.7. | Stanovení obsahu salinomycinu | -A- | 1.8. | Stanovení obsahu salinomycinu | -A- | 1.9. | Stanovení obsahu tylosinu | -A- | 1.10. | Stanovení obsahu virginiamycinu | -A- -B- | 1.11. | Stanovení obsahu zinkbacitracinu | -A- | 1.12. | Stanovení obsahu zinkbacitracinu | -B- | 1.13. | Stanovení obsahu flavofosfolipolu | -B- | 1.14. | Stanovení obsahu avoparcinu | -B- | 1.15. | Stanovení obsahu monensinu | -B- | 1.16. | Stanovení obsahu spiramycinu | -B- | 1.17. | Stanovení obsahu virginiamycinu | -B- |
2. | Antikokciodika | | 2.1. | Stanovení obsahu amprolia | -A- | 2.2. | Stanovení obsahu amprolia | -B- | 2.3. | Stanovení obsahu diclazurilu | -A- | 2.4. | Stanovení obsahu lasalocidu | -A- | 2.5. | Stanovení obsahu maduramicinu | -A- | 2.6. | Stanovení obsahu metylbenzochátu | -A- | 2.7. | Stanovení obsahu narasinu | -A- | 2.8. | Stanovení obsahu narasinu | -A- | 2.9. | Stanovení obsahu nikarbazinu | -A- | 2.10. | Stanovení obsahu nikarbazinu | -B- | 2.11. | Stanovení obsahu robenidinu | -A- -B- | 2.12. | Stanovení obsahu sulfachinoxalinu | -B- | 2.13. | Stanovení obsahu meticlorpindolu | -A- | 2.14. | Stanovení obsahu meticlorpindolu | -B- | 2.15. | Stanovení obsahu kurasanu | -A- | 2.16. | Stanovení obsahu salinomycinu - je uvedeno v Příloze 10, část 1 | | 2.17. | Stanovení obsahu monensinu - je uvedeno v Příloze 10, část 1 | | 2.18. | Stanovení obsahu dinitolmidu | -B- | 2.19. | Stanovení obsahu halofuginonu | -B- | 2.20. | Stanovení obsahu decoquinátu | -B- | 2.21. | Stanovení obsahu arprinocidu | -B- | 2.22. | Stanovení obsahu ethopabátu | -A- | 2.23. | Stanovení obsahu lasalocidu | -A- | 2.24. | Stanovení obsahu semduramicinu | -A- |
3. | Chemoterapeutika | | 3.1. | Stanovení obsahu dimetridazolu | -A- | 3.2. | Stanovení obsahu dimetridazolu | -B- |
4. | Vitaminy | | 4.1. | Stanovení obsahu vitaminu A a vitaminu E | -A- | 4.2. | Stanovení obsahu vitaminu A a vitaminu E | -A- | 4.3. | Stanovení obsahu vitaminu E | -A- | 4.4. | Stanovení obsahu přidaného vitaminu E | -A- | 4.5. | Stanovení obsahu vitaminu E | -A- | 4.6. | Stanovení obsahu cholinu | -A- | 4.7. | Stanovení obsahu pantothenanu vápenatého | -A- | 4.8. | Stanovení obsahu vitaminu B1, B2, B6 | -A- | 4.9. | Stanovení obsahu vitaminu B2 | -A- | 4.10. | Stanovení obsahu vitaminu B6 | -A- | 4.11. | Stanovení obsahu vitaminu K3 | -A- | 4.12. | Stanovení obsahu vitaminu K3 | -B- |
1. | | Stimulátory růstu | | 1.1. | Stanovení obsahu avilamycinu Účel, rozsah, princip Postup specifikuje podmínky pro stanovení obsahu avilamycinu v krmivech a. premixech. Obsah avilamycinu se stanoví difúzním plotnovým postupem na základě inhibičního účinku na růst testovacího mikroorganismu Micrococcus luteus CCM 732 (ATCC 10 240). Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu avilamycinu: | | | od 10 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg./kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg./kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 10 mg/kg. | | 1.2. | Stanovení obsahu avoparcinu Účel, rozsah a princip Používají se tři zkušební postupy, z nichž dva jsou pro stanovení obsahu avoparcinu v premixech bez i za přítomnosti ionoforových antikokcidik. Třetí postup se používá pro stanovení obsahu avoparcinu v krmivech Vzorek se extrahuje směsným rozpouštědlem aceton-voda-kyselina chlorovodíková a obsah avoparcinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu avoparcinu: | | | od 10 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 10 mg/kg. | | 1.3. | Stanovení obsahu flavofosfolipolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení flavofosfolipolu v premixech: Obsah flavofosfolipolu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Staphylococcus aureus CCM 2022 (ATCC 6538) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu flavofosfolipolu nad 200 mg/kg 10 % relat. Mez stanovitelnosti Mez stanovitelnosti je 200 mg/kg. | | 1.4. | Stanovení obsahu olachindoxu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu olachindoxu v krmivech a premixech. Obsah olachindoxu se stanoví po extrakci směsným rozpouštědlem metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV-detekcí. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu olachindoxu: | | | od 5,0 do 15 mg/kg | 25 % relat. | | | od 15 do 100 mg/kg | 15 % relat. | | | od 100 do 1500 mg/kg | 10 % relat. | | | od 1500 do 5000 mg/kg | 150 mg/kg | | | nad 5000 mg/kg | 3 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit pří obsahu olachindoxu: | | | od 5,0 do 12 mg/kg | 50 % relat. | | | od 12 do 40 mg/kg | 6 mg/kg | | | od 40 do 300 mg/kg | 15 % relat. | | | od 300 do 450 mg/kg | 45 mg/kg | | | od 450 do 5000 mg/kg | 10 % relat. | | | od 5000 do 10000 mg/kg | 500 mg/kg | | | nad 10000 mg/kg | 5 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 5,0 mg/kg. | | 1.5. | Stanovení obsahu monensinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu monensinu v krmivech a premixech. Obsah monensinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu monensinu: | | | od 20 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 20 mg/kg. | | 1.6. | Stanovení obsahu monensinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu monensinu v krmivech a premixech. Obsah monensinu se stanoví po extrakci směsným rozpouštědlem, extrakt je přečištěn na pevné fázi a takto přečištěný extrakt je rozpuštěn v definovaném objemu mobilní fáze. Monensin se stanovuje metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi a po postkolonové derivatizaci s p-dimethylaminobenzaldehydem při 90 °C je detekován UV-detektorem pří vlnové délce 600 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu monensinu: | | | od 0,2 do 30 mg/kg | 15 % relat. | | | od 30 do 90 mg/kg | 4,5 mg/kg | | | nad 90 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 0,2 mg/kg. | | 1.7. | Stanoveni obsahu salinomycinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení salinomycinu v krmivech a premixech. Obsah salinomycinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu salinomycinu: | | | od 10 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 10 mg/kg. | | 1.8. | Stanovení obsahu salinomycinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu salinomycinu v krmivech a premixech. Obsah salinomycinu se stanoví po extrakci směsným rozpouštědlem, extrakt je přečištěn na pevné fázi a takto přečištěný extrakt je rozpuštěn v definovaném objemu mobilní fáze. Salinomycin se stanovuje metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi a po postkolonové derivatizaci s p-dimethylaminobenzaldehydem při 90 °C je detekován UV-detektorem při vlnové délce 600 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu salinomycinu: | | | od 1,4 do 25 mg/kg | 20 % relat. | | | od 25 do 100 mg/kg | 5 mg/kg | | | nad 100 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,4 mg/kg. | | 1.9. | Stanovení obsahu tylosinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení tylosinu v krmivech a premixech od obsahu nad 10 mg/kg. Obsah tylosinu se stanoví po extrakci vzorku ethylalkoholem na základě inhibičního účinku na růst testovacího mikroorganismu Micrococcus varians CCM 552 (ATCC 9341) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí pro všechny obsahy tylosinu překročit 10 % relativních. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu tylosinu: | | | od 10 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti ke 10 mg/kg. | | 1.10. | Stanovení obsahu virginiamycinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení virginiamycinu v krmivech a premixech. Vzorek je extrahován směsí kyseliny citrónové a acetonu a obsah virginiamycinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Micrococcus varians CCM 552 (ATCC 9341 ) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděními na stejném vzorku nesmí pro všechny obsahy virginiamycinu překročit 10 % relativních. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu virginiamycinu: | | | od 5 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Nestanovena. | | 1.11. | Stanovení obsahu zinkbacitracinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení zinkbacitracinu v premixech. Obsah zinkbacitracinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Micrococcus luteus CCM 732 (ATCC 10 240) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 200 mg/kg. | | 1.12. | Stanovení obsahu zinkbacitracinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení zinkbacitracinu v krmivech a premixech. Obsah zinkbacitracinu se stanoví po extrakci vzorku směsí okyseleného zředěného roztoku methylalkoholu na základě inhibičního účinku na růst testovacího mikroorganismu Micrococcus luteus CCM 732 (ATCC 10 240) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu zinkbacitracinu: | | | od 5,0 do 10 mg/kg | 2 mg/kg | | | od 10 mg/kg do 25 mg/kg | 20 % relat. | | | od 25 mg/kg do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu zinkbacitracinu: | | | od 5,0 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 100 mg/kg | 20 % relat. | | | od 100 do 200 mg/kg | 20 mg/kg | | | nad 200 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 5,0 mg/kg. | | 1.13. | Stanovení obsahu flavofosfolipolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení flavofosfolipolu v krmivech a premixech. Obsah flavofosfolipolu po extrakci vzorku zředěným methylalkoholem se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Staphylococcus aureus CCM 2022 (ATCC 6538) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu flavofosfolipolu: | | | od 1,0 do 2,0 mg/kg | 0,5 mg/kg | | | od 2,0 do 10 mg/kg | 25 % relat. | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,0 mg/kg. | | 1.14. | Stanovení obsahu avoparcinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení avoparcinu v krmivech a premixech. Obsah avoparcinu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu avoparcinu: | | | od 2,0 do 10 mg/kg | 2 mg/kg | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 2,0 mg/kg. | | 1.15. | Stanovení obsahu monensinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu monensinu v krmivech a premixech. Obsah monensinu se stanoví na základě jeho inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu monensinu: | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 10 mg/kg. | | 1.16. | Stanovení obsahu spiramycinu Účel, rozsah a princip Postup specifikuje podmínky pro stanoveni obsahu spiramycinu v krmivech a premixech. Obsah spiramycinu se stanoví na základě jeho inhibičního účinku na růst testovacího mikroorganismu Micrococcus luteus CCM 552 (ATCC 9341 ) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu spiramycinu: | | | od 1,0 do 10 mg/kg | 2 mg/kg | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,0 mg/kg. | | 1.17. | Stanovení obsahu virginiamycinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu virginiamycinu v krmivech a premixech. Obsah virginiamycinu se po extrakci vzorku methylalkoholickým roztokem smáčedla (Tween) stanoví na základě jeho inhibičního účinku na růst testovacího mikroorganismu Micrococcus luteus CCM 732 (ATCC 10240) difúzním plotnovým postupem. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu virginiamycinu: | | | od 2,0 do 10 mg/kg | 2 mg/kg | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 2,0 mg/kg. | 2. | | Antikocidika | | 2.1. | Stanovení obsahu amprolia Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu amprolia v krmivech a premixech. Obsah amprolia se stanoví po extrakci methylalkoholem a přečištění na pevné fázi metodou vysokoúčinné kapalinové chromatografie na reverzní fázi s UV - detekcí při vlnové délce 270 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu amprolia : | | | od 1,3 do 30 mg/kg | 15 % relat. | | | od 30 do 60 mg/kg | 4,5 mg/kg | | | od 60 do 120 mg/kg | 7,5 % relat. | | | od 120 do 180 mg/kg | 9 mg/kg | | | nad 180 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,3 mg/kg. | | 2.2. | Stanovení obsahu amprolia Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu amprolia v krmivech a premixech pro obsah nad 40 mg/kg. Obsah amprolia se stanoví po extrakci methylalkoholem a po přečištění extraktu na oxidu hlinitém. Vzniklý barevný komplex po působení činidla (hydroxid sodný, 2,7-dihydroxynaftalen hexakyanoželezitan draselný a kyanid draselný) se proměří spektrofotometricky při vlnové délce 530 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu amprolia: | | | od 40 do 100 mg/kg | 10 mg/kg | | | od 100 do 5000 mg/kg | 10 % relat. | | | od 5 000 do 10 000 mg/kg | 500 mg/kg | | | nad 10 000 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 40 mg/kg. | | 2.3. | Stanovení obsahu diclazurilu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu diclazurilu v krmivech a premixech. Obsah diclazurilu se stanoví po extrakci vzorku okyseleným methylalkoholem a přečištění na pevné fázi metodou vysokoúčinné kapalinové chromatografie na reverzní fázi s použitím UV detekce při vlnové délce 280 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 0,7 mg/kg. | | 2.4. | Stanovení obsahu lasalocidu Účel, rozsah a princip Postup specifikuje podmínky pro stanoveni obsahu lasalocidu v premixech. Obsah lasalocidu se stanoví na základě inhibičního účinku na růst testovacího mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 20 mg/kg. | | 2.5. | Stanovení obsahu maduramicinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu maduramicinu v premixech. Obsah maduramicinu se stanoví po extrakci vzorku směsí acetonitrilu a dichlormethanu, předkolonové derivatizaci dansylchloridem a následném přečištění na pevné fázi metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s použitím fluorimetrické detekce (excitační vlnová délka 224 nm; emisní vlnová délka 515 nm) nebo UV detekce při vlnové délce 224 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 8 mg/kg. | | 2.6. | Stanovení obsahu methylbenzochátu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu methylbenzochátu v krmivech a premixech. Obsah methylbenzochátu se stanoví po extrakci vzorku methylalkoholovým roztokem methansulfonové kyseliny, po přečištění extrakcí dichlormethanem je izolován na chromatografickém ionexovém sloupci a znovu extrahován dichlormethanem, nakonec stanoven metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV detekcí nebo FF detekcí (excitační vlnová délka 265 nm, emisní vlnová délka 390 nm). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu methylbenzochátu od 4,0 do 20 mg/kg hodnotu 10% relat. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,0 mg/kg pro UV detekci a 0,5 mg/kg pro FF detekci. | | 2.7. | Stanovení obsahu narasinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu narasinu v premixech. Obsah narasinu se stanoví na základě inhibičního účinku na růst testovacího, mikroorganismu Bacillus subtilis CCM 1999 (ATCC 6633) difúzním plotnovým postupem. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 20 mg/kg. | | 2.8. | Stanovení obsahu narasinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu narasinu v krmivech a premixech. Obsah narasinu se stanoví po extrakci směsným rozpouštědlem, extrakt je přečištěn na pevné fázi a takto přečištěný extrakt je rozpuštěn v definovaném objemu mobilní fáze. Narasin se stanoví metodou vysokoúčinné kapalinové chromatografie na reverzní fázi a po postkolonové derivatizaci s p-dimethylaminobenzaldehydem při 90 °C je detekován UV-detektorem při vlnové délce 600 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 0,7 mg/kg. | | 2.9 | Stanovení obsahu nikarbazinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení nikarbazinu v krmivech a premixech. Obsah nikarbazinu se stanoví spektrofotometricky po extrakci n-hexanem a chromatografické separaci v prostředí alkalického roztoku chloridu draselného. Opakovatelnost. Nestanovená Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 2.10. | Stanovení obsahu nikarbazinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení nikarbazinu v krmivech a premixech. Obsah nikarbazinu se stanoví po extrakci dimethylformamidem spektrofotometricky při 430 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu nikarbazinu: | | | od 20 do 100 mg/kg | 10 mg/kg | | | od 100 do 5 000 mg/kg | 10 % relat. | | | od 5 000 do 10 000 mg/kg | 500 mg/kg | | | nad 10 000 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 20 mg/kg. | | 2.11. | Stanovení obsahu robenidinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu robenidinu v krmivech a premixech. Obsah robenidinu se stanoví po extrakci vzorku okyseleným methylalkoholem, jeho přečištění na alumině A, metodou vysokoúčinné kapalinové chromatografie na reverzní fázi s použitím UV detekce při vlnové délce 347 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu robenidinu vyšším než 15 mg/kg hodnotu 10 % relat. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu robenidinu: | | | od 3,1 do 10 mg/kg | 2 mg/kg | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | od 50 do 5000 mg/kg | 10 % relat. | | | od 5000 do 10000 mg/kg | 500 mg/kg | | | nad 10000 mg/kg | 5 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 3,1 mg/kg. | | 2.12 | Stanovení obsahu sulfaquinoxalinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení sulfaquinoxalinu v krmivech a premixech. Mez stanovitelnosti je 20 mg/kg. Vzorek se extrahuje roztokem dimethyformamidu s chloroformem a obsah sulfaquinoxalinu se stanoví po jeho alkalické hydrolýze, diazotaci a kopulaci N-2-aminoethyl-1-naftylaminem, spektrofotometricky při vlnové délce 545 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu sulfoquinoxalinu: | | | 20 až 100 mg/kg | 10 mg/kg | | | 100 až 5 000 mg/kg | 10 % relat. | | | 5 000 až 10 000 mg/kg | 500 mg/kg | | | nad 10 000 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 2.13. | Stanovení obsahu meticlorpindolu (clopidol, coyden) Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu meticlorpindolu v krmivech a premixech. Obsah meticlorpindolu se stanoví po extrakci vzorku směsným rozpouštědlem methylalkohol-amoniak a po jeho převedení do mobilní fáze metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV detekcí při 265 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 3,6 mg/kg. | | 2.14. | Stanovení obsahu meticlorpindolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu meticlorpindolu v krmivech a premixech. Obsah meticlorpindolu s. stanoví po extrakci vzorku směsným rozpouštědlem methylalkohol-chloroform-amoniak, následném přečištění chromatografií na pevné fázi na oxidu hlinitém a na ionexu spektrofotometricky při vlnových délkách 267, 297 a 327 nm s ohledem na korekci pozadí. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu meticlorpindolu: | | | od 30 do 100 mg/kg | 5 mg/kg | | | nad 100 mg/kg | 5 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu meticlorpindolu: | | | od 30 do 100 mg/kg | 15 mg/kg | | | od 100 do 300 mg/kg | 15 % relat. | | | od 300 do 450 mg/kg | 45 mg/kg | | | od 450 do 5000 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 30 mg/kg. | | 2.15. | Stanovení obsahu kurasanu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení kurasanu v premixech. Obsah kurasanu se stanoví po extrakcí hexanem spektrofotometricky v ÚV oblasti při vlnové délce 361 nm. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 2.16. | Stanovení obsahu salinomycinu Postup stanovení obsahu salinomycinu uvedena v příloze č. 10, část 1. | | 2.17. | Stanovení obsahu monenzinu Postup stanovení obsahu monenzinu je uvedena v příloze č. 10, část 1. | | 2.18. | Stanovení obsahu dinitolmidu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu dinitolmidu v krmivech a premixech. Mez stanovitelnosti je 40 mg/kg. Obsah dinitolmidu se stanoví po extrakci vzorku acetonitrilem spektrofotometricky při vlnové délce 560 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu dinitolmidu hodnotu: | | | pod 100 mg/kg | 10 mg/kg | | | od 100 do 5 000 mg/kg | 10 % relat. | | | od 5 000 do 10 000 mg/kg | 500 mg/kg | | | nad 10 000 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 40 mg/kg. | | 2.19. | Stanovení obsahu halofuginonu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu halofuginonu v krmivech a premixech. Obsah halofuginonu se stanoví po extrakci horkou vodou a přečištění na ionexu metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV - detekcí při vlnové délce 243 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu halofuginonu do 3,0 mg/kg hodnotu 0,5 mg/kg. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,0 mg/kg. | | 2.20. | Stanovení obsahu decoquinátu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu decoquinátu v krmivech. Vzorek se extrahuje methylalkoholickým roztokem chloridu vápenatého a obsah decoquinátu stanoví se fluorometricky. Opakovatelnost. Nestanovena Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 2.21. | Stanovení obsahu arprinocidu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu arprinocidu v krmivech. Vzorek se extrahuje chloroformem a obsahu arprinocidu je stanoven vysokoúčinnou kapalinovou chromatografií (HPLC) s UV detekcí při 254 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 2.22. | Stanovení obsahu ethopabátu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu ethopabátu v krmivech a premixech. Obsah ethopabátu se stanoví po extrakci vzorku methylalkoholem a přečištění chromatografií na pevné fázi na alumině B metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s fluorescenční detekcí (excitační vlnová délka 268 nm; emisní vlnová délka 350 nm). Výsledky se vyjadřují pro obsah: | | | od 0,03 do 1,0 mg/kg | s přesností na 0,01 mg/kg | | | od 1,1 do 10 mg/kg | s přesností na 0,1 mg/kg | | | od 10,1 do 1000 mg/kg | s přesností na 1 mg/kg | | | od 1001 do 10 000 mg/kg | s přesností na 10 mg/kg | | | od 10 001 do 100 000 mg/kg | s přesností na 100 mg/kg | | | nad 100 000 mg/kg | s přesností na 1000 mg/kg | | | Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu ethopabátu: | | | od 0,03 do 1,0 mg/kg | 40 % relat. | | | od 1,0 do 4,0 mg/kg | 0,4 mg/kg | | | od 4,0 do 20 mg/kg | 10 % relat. | | | od 20 do 1000 mg/kg | nestanovena | | | nad 1000 mg/kg | 5 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu ethopabátu: | | | od 0,03 do 1,0 mg/kg | nestanovena | | | od 1,0 do 20 mg/kg | 20 % relat. | | | od 20 od 1000 mg/kg | nestanovena | | | nad 1000 mg/kg | 15 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 0,03 mg/kg. | | 2.23. | Stanovení obsahu lasalocidu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu lasalocidu v krmivech a premixech. Obsah lasalocidu se stanoví po extrakci vzorku methylalkoholem a jeho převedení do mobilní fáze metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s fluorescenční detekcí při excitační vlnové délce 310 nm a emisní vlnové délce 419 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu lasalocidu: | | | od 0,4 do 20 mg/kg | 20% relat. | | | od 20 do 40 mg/kg | 4 mg/kg | | | nad 40 mg/kg | 10% relat. | | | Uvedené hodnoty opakovatelnosti se nevztahují pro určení pracovní přesnosti míchacího zařízení podle přílohy č. 16. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu lasalocidu: | | | od 0,4 do 50 mg/kg | 30 % relat. | | | od 50 do 75 mg/kg | 15 mg/kg | | | nad 75 mg/kg | 20 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 0,4 mg/kg. | | 2.24. | Stanovení obsahu semduramicinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu semduramicinu v krmivech a premixech. Obsah semduramicinu se stanoví po extrakci směsným rozpouštědlem hexan-octan ethylnatý a extrakt je přečištěn na pevné fázi a takto přečištěný extrakt je rozpuštěn v definovaném objemu mobilní fáze. Semduramicin se stanoví metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fází a po postkolonové derivatizaci s vanilinem při 90 °C je detekován UV-detektorem při vlnové délce 522 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 3. | | Chemoterapeutika | | 3.1. | Stanovení obsahu dimetridazolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu dimetridazolu v krmivech a premixech. Obsah dimetridazolu se stanoví po extrakci vzorku 90 % methylalkoholem a přečištění chromatografií na pevné fázi na alumině B metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV detekcí při 309 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu dimetridazolu: | | | od 3,0 do 30 mg/kg | 15 % relat. | | | od 30 do 100 mg/kg | 5 mg/kg | | | nad 100 mg/kg | 5 % relat. | | | Uvedené hodnoty opakovatelnosti se nevztahují pro určení pracovní přesnosti míchacího zařízení podle přílohy č. 16. Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu dimetridazolu: | | | od 3,0 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | nad 50 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je 3,0 mg/kg. | | 3.2. | Stanovení obsahu dimetridazolu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu dimetridazolu v krmivech. Obsah dimetridazolu se stanoví po extrakci vzorku methanolem a přečištění na alumině spektrofotometricky. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu dimetridazolu: | | | do 4,0 mg/kg | 50 % relat. | | | od 4,0 do 10 mg/kg | 2 mg/kg | | | od 10 do 25 mg/kg | 20 % relat. | | | od 25 do 50 mg/kg | 5 mg/kg | | | od 50 do 5000 mg/kg | 10 % relat. | | | od 5000 do 10000 mg/kg | 500 mg/kg | | | nad 10 000 mg/kg | 5 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 4. | | Vitaminy | | 4.1. | Stanovení obsahu vitaminu A a vitaminu E Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu A a vitaminu E v krmivech a premixech. Obsah vitaminu A a E se stanoví po alkalické hydrolýze hydroxidem draselným a následné extrakci na pevné fázi po převedení do cyklohexanu metodou vysokoúčinné kapalinové chromatografie (HPLC) na normální fázi s UV detekcí při 325 nm nebo fluorescenční detekcí (excitační vlnová délka 325 nm, emisní vlnová délka 480 nm) pro vitamin A a UV detekce při 292 nm nebo fluorescenční detekcí (excitační vlnová délka 292 nm, emisní vlnová délka 330 nm) pro vitamin E. Výsledky se vyjadřují pro obsah vitaminu A: | | | do 999 m.j./kg | s přesností na 1 m.j./kg | | | do 1000 do 9999 m.j./kg | s přesností na 10 m.j./kg | | | od 10000 do 99999 m.j./kg | s přesností na 100 m.j./kg | | | od 100000 do 999999 m.j./kg | s přesností na 1000 m.j./kg | | | nad 1000000 m.j./kg | s přesností na 10000m.j./kg | | | Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu A (UV detekce): | | | od 1000 do 50000 m.j./kg | 20 % relat. | | | od 50000 do 100000 m.j./kg | 10000 m.j./kg | | | nad 100000 m.j./kg | 10 % relat. | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 50 mg/kg | 20 % relat. | | | od 50 do 100 mg/kg | 10 mg/kg | | | nad 100 mg/kg | 10 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu A (UV detekce): | | | od 1000 do 4000 m.j./kg | 1000 m.j./kg | | | od 4000 do 100000 m.j./kg | 25 % relat. | | | od 100000 do 125000 m.j./kg | 25000 m.j./kg | | | od 125000 do 375000 m.j./kg | 20 % relat. | | | od 375000 do 600000 m.j./kg | 75000 m.j./kg | | | od 600000 do 800000 m.j./kg | 12,5 % relat. | | | od 800000 do 1000000 m.j./kg | 100000 m.j./kg | | | nad 1000000 m.j./kg | 10 % relat. | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 150 mg/kg | 20 % relat. | | | od 150 do 200 mg/kg | 30 mg/kg | | | od 200 do 500 mg/kg | 15 % relat. | | | od 500 do 750 mg/kg | 75 mg/kg | | | nad 750 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti pro vitamin A je 250 m.j./kg pro fluorescenční detekci, pro UV detekci 1000 m.j./kg. Mez stanovitelnosti pro vitamin E je 0,1 mg/kg pro fluorescenční detekci, pro UV detekci 0,8 mg/kg. | | 4.2. | Stanovení obsahu vitaminu A a vitaminu E Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu A a vitaminu E v krmivech a premixech. Obsah vitaminu A a E se stanoví po alkalické hydrolýze hydroxidem draselným a následné extrakci hexanem a převedením do methylalkoholu metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV detekcí při 325 nm nebo fluorescenční detekcí (excitační vlnová délka 325 nm, emisní vlnová délka 480 nm) pro vitamin A a UV detekce při 292 nm nebo fluorescenční detekcí (excitační vlnová délka 292 nm, emisní vlnová délka 330 nm) pro vitamin E. Výsledky se vyjadřují pro obsah vitaminu A: | | | do 999 m.j./kg | s přesností na 1 m.j./kg | | | do 1000 do 9999 m.j./kg | s přesností na 10 m.j./kg | | | od 10000 do 99999 m.j./kg | s přesností na 100 m.j./kg | | | od 100000do 999999 m.j./kg | s přesností na 1000 m.j./kg | | | nad 1000000 m.j./kg | s přesností na 10000m.j./kg | | | Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu A (UV detekce): | | | od 1000 do 8000 m.j./kg | 25 % relat. | | | od 8000 do 13500 m.j/kg | 2000 m.j./kg | | | od 13500 do 40000 m.j./kg | 15 % relat. | | | od 40000 do 300000 m.j./kg | 37500 m.j./kg | | | od 300000 do 1600000 m.j./kg | 12,5 % relat. | | | od 1600000 do 2600000 m.j./kg | 200000 m.j./kg | | | od ?600000 do 4000000 m.j./kg | 7,5 % relat. | | | Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do55 mg/kg | 10 % relat. | | | od 55 do 100 mg/kg | 5,5 mg/kg | | | od 100 do 250 mg/kg | 5,5 % relat. | | | od 500 do 1000 mg/kg | 45 mg/kg | | | od 1000 do 5000 mg/kg | 4,5 % relat. | | | od 5000 do 7500 mg/kg | 225 mg/kg | | | více než 7500 mg/kg | 3 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu A (UV detekce): | | | od 1000 do 100000 m.j./kg | 25 % relat. | | | od 100000 do 125000 m.j./kg | 25000 m.j./kg | | | od 125000 do 375000 m.j./kg | 20 % relat. | | | od 375000 do 600000 m.j./kg | 75000 m.j./kg | | | od 600000 do 800000 m.j./kg | 12,5 % relat. | | | od 800000 do 1000000 m.j./kg | 100000 m.j./kg | | | nad 1000000 m.j./kg | 10 % relat. | | | Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 mg/kg do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 150 mg/kg | 20 % relat. | | | od 150 do 200 mg/kg | 30 mg/kg | | | od 200 do 500 mg/kg | 15 % relat. | | | od 500 do 750 mg/kg | 75 mg/kg | | | nad 750 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti pro vitamin A je 250 m.j./kg pro fluorescenční detekci, pro UV detekci 1000 m.j./kg. Mez stanovitelnosti pro vitamin E je 0,1 mg/kg pro fluorescenční detekci, pro UV detekci 0,8 mg/kg. | | 4.3. | Stanovení obsahu vitaminu E Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu E v krmivech a premixech. Obsah vitaminu E se stanoví po alkalické hydrolýze hydroxidem draselným a následné extrakci na pevné fázi po převedení do cyklohexanu metodou vysokoúčinné kapalinové chromatografie (HPLC) na normální fázi s UV detekcí při 292 nm nebo fluorescenční detekcí (excitační vlnová délka.295 nm, emisní vlnová délka 330 nm). Opakovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 50 mg/kg | 20 % relat. | | | od 50 do 100 mg/kg | 10 mg/kg | | | nad 100 mg/kg | 10 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 150 mg/kg | 20 % relat. | | | od 150 do 200 mg/kg | 30 mg/kg | | | od 200 do 500 mg/kg | 15 % relat. | | | od 500 do 750 mg/kg | 75 mg/kg | | | nad 750 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je pro UV detekci 0,8 mg/kg, pro fluorescenční detekci 0,1 mg/kg. | | 4.4. | Stanovení obsahu přidaného vitaminu E Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu E v premixech a v krmných směsích. Obsah přidaného vitaminu E (octan tokoferolu) se stanoví plynovou chromatografií po extrakci vzorku diethyletherem resp. hexanem přímo, resp. po přečištění na sloupci oxidu hlinitého. Opakovatelnost Pro premixy: Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí při obsahu vitaminu E 1500 000 mg/kg překročit hodnotu 88000 mg/kg. Pro krmné směsi: Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí při obsahu vitaminu E 20 mg/kg překročit hodnotu 2,15 mg/kg. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 4.5. | Stanovení obsahu vitaminu E Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu E v krmivech a premixech. Obsah vitaminu E se stanoví po alkalické hydrolýze hydroxidem draselným a následné extrakci hexanem a převedením do methylalkoholu metodou vysokoúčinné kapalinové chromatografie (HPLC) na reverzní fázi s UV detekcí při 292 nm nebo fluorescenční detekcí (excitační vlnová délka 295 nm, emisní vlnová délka 330 nm). Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 55 mg/kg | 10 % relat. | | | od 55 do 100 mg/kg | 5,5 mg/kg | | | od 100 do 250 mg/kg | 5,5 % relat. | | | od 500 do 1000 mg/kg | 45 mg/kg | | | od 1000 do 5000 mg/kg | 4,5 % relat. | | | od 5000 do 7500 mg/kg | 225 mg/kg | | | více než 7500 mg/kg | 3 % relat. | | | Reprodukovatelnost Rozdíl mezi dvěma výsledky zkoušek stejného vzorku prováděnými ve dvou laboratořích nesmí překročit při obsahu vitaminu E (UV detekce): | | | od 0,8 do 25 mg/kg | 40 % relat. | | | od 25 do 50 mg/kg | 10 mg/kg | | | od 50 do 150 mg/kg | 20 % relat. | | | od 150 do 200 mg/kg | 30 mg/kg | | | od 200 do 500 mg/kg | 15 % relat. | | | od 500 do 750 mg/kg | 75 mg/kg | | | nad 750 mg/kg | 10 % relat. | | | Mez stanovitelnosti Mez stanovitelnosti je pro UV detekci 0,8 mg/kg, pro fluorescenční detekci 0,1 mg/kg. | | 4.6. | Stanovení obsahu cholinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu cholinu v krmivech a premixech. Obsah cholinu se stanoví po hydrolýze vzorku hydroxidem barnatým a přečištění hydrolyzátu na ionexu na základě vzniku komplexu s reineckátem amonným v prostředí roztoku fosforečnanu sodného spektrofotometricky po rozpuštění komplexu v acetonu při vlnové délce 525 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 20 mg/kg. | | 4.7. | Stanovení obsahu pantothenanu vápenatého Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu pantothenanu vápenatého v premixech. Obsah pantothenanu vápenatého se stanoví na základě stimulačního účinku na růst testovacího mikroorganismu Saccharomyces carlsbergensis CCM 4288 (ATCC 9080) difúzním plotnovým postupem. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 4.8. | Stanovení vitaminů B1, B2, B6 Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminů B1, B2 a B6 v krmných směsích. Vitaminy B1 (thiamin), B2 (riboflavin) a B6 (pyridoxin) se extrahují ze vzorku krmiva vodou a po hydrolýze kyselinou chloristou se stanoví postupem vysokoúčinné kapalinové chromatografie (HPLC) s využitím iontových párů na reverzní fázi. Detekce vitaminu B2 a B6 se provádí přímo fluorimetricky, zatímco vitamin B1 se před detekcí nejprve oxiduje derivatizačním činidlem v reakční smyčce postkolonové derivatizace. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 4.9. | Stanovení obsahu vitaminu B2 Účel, rozsah a princip Používají se dva postupy stanovení obsahu vitaminu B2 v premixech - postup fluorimetrický a postup difúzní plotnový. Obsah vitamin B2 se stanoví fluorimetricky v mírně okyseleném prostředí na základě fluorescence při vlnové délce 440 nm nebo difúzním plotnovým postupem na základě stimulačního účinku na růst testovacího mikroorganismu Lactobacillus rhamnosus CCM 1825 (ATCC 7469 ). Opakovatelnost Pro metodu fluorometrickou nestanovena. Pro metodu difuzní plotnovou: Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí při obsahu vitaminu B2 500000 mg/kg překročit hodnotu 40500 mg/kg. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 4.10. | Stanovení obsahu vitaminu B6 Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu B6v premixech. Vitamin B6 ve všech jeho formách se stanoví na základě stimulačního účinku na růst testovacího mikroorganismu kvasinky Saccharomyces carlsbergensis CCM 4228 (ATCC 9080) difúzním plotnovým způsobem. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 4.11 | . Stanovení obsahu vitaminu K3 Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu K3 v krmivech a premixech. Obsah vitaminu K3 se stanoví po extrakci vzorku chloroformem, následné hydrolýze amoniakem, metodou vysokoúčinné kapalinové chromatografie (HPLC) na normální fázi s UV detekci při 264 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 2,9 mg/kg. | | 4.12. | Stanovení obsahu vitaminu K3 Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu vitaminu K3 v premixech a krmných směsích. Mez stanovitelnosti je 1,0 mg/kg. Po extrakci vzorku ethylalkoholem se stanoví obsah vitaminu K3 spektrofotometricky při vlnové délce 635 nm. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu vitaminu K3: | | | do 10 mg/kg | 20 % relat. | | | od 10 do 14 mg/kg | 2 mg/kg | | | od 14 do 100 mg/kg | 15 % relat | | | od 100 do 150 mg/kg | 15 mg/kg | | | nad 150 mg/kg | 10 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Mez stanovitelnosti je 1,0 mg/kg. | 5. | | Mikroprvky | | 5.1. | Stanovení obsahu mědi, železa, manganu a zinku Postup stanovení obsahu mědi, železa, manganu a zinku je uvedena v příloze č. 9, část 8. | | 5.2. | Stanovení obsahu kobaltu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu kobaltu v krmivech. Stanovení je založeno na principu tvorby barevného komplexu kobaltu s 2-nitroso-1-naftolem jehož absorbance se měří spektrofotometricky. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu kobaltu: | | | do 5,0 mg/kg | 50 % relat. | | | od 5,0 do 10 mg/kg | 2,5 mg/kg | | | od 10 do 30 mg/kg | 25 % relat. | | | od 30 do 50 mg/kg | 7,5 mg/kg | | | nad 50 mg/kg | 15 % relat. | | | Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 5.3. | Stanovení obsahu selenu. Účel, rozsah a princip Postup specifikuje podmínky pro stanovení selenu v krmivech. Ve vzorku se po rozkladu kyselinou dusičnou v uzavřeném systému stanoví obsah selenu metodou atomové absorpční spektrometrie (AAS) s hydridovou technikou. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 5.4. | Stanovení obsahu jodu Účel, rozsah a princip Používají se dva zkušební postupy. Po mineralizaci vzorku za přídavku hydroxidu sodného jako fixativa při 520 °C se jodidy oxidují v alkalickém prostředí bromnanem a vzniklé jodičnany se stanovují metodou diferenční pulzní rozpouštěcí voltametrie. Postup je vhodný pro stanovení jodu v krmivech a premixech. Pro stanovení jodu v premixech se vzorek mineralizuje po přídavku hydroxidu sodného jako fixativa při 520 °C a jodidy se zoxidují manganistanem draselným na jodičnany. Po přidání jodidu draselného se uvolní jod, který se stanoví titrací thiosíranem sodným. Opakovatelnost Rozdíl mezi dvěma paralelními voltametrickými stanoveními prováděnými na stejném vzorku nesmí překročit při obsahu jodu: | | | od 0;5 do 5,0 mg/kg | 30 % relat. | | | od 5,0 do 15 mg/kg | 1,5 mg/kg | | | nad 15 mg/kg | 10 % relat. | | | Opakovatelnost pro titrační metodu nestanovena. Reprodukovatelnost Nestanovena Mez stanovitelnosti Mez stanovitelnosti pro voltametrickou metodu je 0,5 mg/kg. Pro titrační metodu mez stanovitelnosti nestanovena. | 6. | | Vehikula a pojiva | | 6:1. | Stanovení obsahu oxidu křemičitého Postup stanovení obsahu oxidu křemičitého je uveden v příloze č. 9, část 7. | | 6.2. | Stanovení obsahu oxidu hlinitého Postup stanovení obsahu oxidu hlinitého je uveden v příloze č. 9, část 7. | 7. | | Výpočty | | 7.1. | Vyhodnocování a výpočet výsledků stanovení obsahu doplňkových látek pro difúzní plotnové postupy Účel; rozsah a princip Postup uvádí a specifikuje uzančně závazný způsob pro vyhodnocování a výpočet výsledků při stanovení obsahu doplňkových látek v krmivech a premixech pro difuzní plotnové postupy. Průměry inhibičních resp. stimulačních zón, vzniklých při stanovení doplňkových látek difuzním plotnovým postupem, se měří pomocí odpichovátka s přesností nejméně na 0,1 mm. Ze souboru takto získaných hodnot se vypočítá aritmetický průměr pro každou koncentraci zkoušeného vzorku i standardu. | 8. | | Antioxidanty | | 8.1. | Stanovení obsahu ethoxyquinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení ethoxyquinu v krmivech. Ethoxyquin je ze vzorku extrahován methylalkoholem a alikvotní podíl extraktu je po zředění vodou reextrahován do petroletheru a obsah ethoxyquinu je stanoven fluorimetricky. Opakovatelnost Nestanovena Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 8.2. | Stanovení obsahu butylhydroxytoluenu, butylhydroxyanisolu a galátů Účel; rozsah a princip Postup specifikuje podmínky pro stanovení obsahu butylhydroxytoluenu, butylhydroxyanisolu a galátů v tucích. Vzorek se rozpustí v hexanu a butylhydroxytoluen, butylhydroxyanisol a galáty se extrahují acetonitrilem. Vlastní stanovení se provádí postupem vysokoúčinné kapalinové chromatografie (HPLC) s použitím UV detekce při 280 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 9. | | Barviva | | 9.1. | Stanovení obsahu kapsatinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení celkového obsahu barviva vyjádřeného jako kapsatin, převažujícího barviva papriky. Obsah kapsatinu se stanoví po extrakci vzorku benzenem způsobem podle Benedikta spektrofotometricky. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 9.2. | Stanovení obsahu nativních a přidaných karotenoidů Účel, rozsah a princip Používají se dva postupy. Jeden specifikuje podmínky pro stanovení obsahů esterů kyseliny apo-karotinové, citranaxantinu a kantaxantinu, druhý specifikuje podmínky pro stanovení obsahu karoténů, veškerých xantofylů, luteinu a zeaxantinu. Vzorek se extrahuje rozpouštědlem, přečistí se postupem sloupcové chromatografie a obsah příslušného barviva se stanoví spektrofotometricky. Opakovatelnost Rozdíl mezi dvěma paralelními stanoveními prováděnými na stejném vzorku nesní překročit 15 % relat. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 10. | | Konzervanty | | 10.1. | Stanovení obsahu kyseliny mravenčí Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu kyseliny mravenčí v silážích. Kyselina mravenčí se stanovuje postupem podle Fuchse. Těkavé kyseliny, vydestilované ze vzorku se podrobí reakci s manganistanem draselným. Kyselina mravenčí je jako jedinná oxidována v neutrálním nebo slabě alkalickém prostředí. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 10.2. | Stanovení obsahu kysličníku siřičitého Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu kysličníku siřičitého v krmivech. Kysličník siřičitý se uvolní po okyselení vzorku krmiva proudem dusíku a jímá se do roztoku elektrolytu. Obsah kysličníku siřičitého se stanoví metodou diferenční pulzní polarografie. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | | 10.3. | Stanovení obsahu formaldehydu Účel, rozsah a princip Postup specifikuje podmínky pro stanoveni obsahu formaldehydu v krmivech. Ze vzorku se po okyselení kyselinou fosforečnou izoluje formaldehyd destilací s vodní parou a formaldehyd se v destilátu stanoví po reakci s kyselinou chromotropovou fotometricky při 570 nm. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 11: | | Zchutňovadla | | 11.1. | Stanovení obsahu sacharinu Účel, rozsah a princip Postup specifikuje podmínky pro stanovení obsahu sacharinu v krmivech. Sacharin se extrahuje z vodného roztoku krmiva chloroformem a jeho obsah se stanoví metodou diferenční pulsní polarografie. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. Mez stanovitelnosti Nestanovena. | 12. | | Mikrobiotika | | 12.1. | Stanovení počtu zárodků bakterií kmene Streptococcus Účel, rozsah a princip Postup specifikuje podmínky pro stanovení počtu zárodků kmene Streptococcus skupiny D v krmivech a premixech. Stanovení počtu zárodků, bakterií kmene Streptococcus se provádí na selektivních půdách podle Slanetze a Bartleye. Jako referenční půda se při stanovení používá další selektivní půda (např. KF agar) nebo u premixů vhodná neselektivní půda. Naočkované půdy jsou kultivovány při 37°C ± 1°C. Růst.a počty kolonií se vyhodnocují po dvou a čtyřdenní kultivaci. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena. | | 12.2. | Stanovení počtu zárodků bakterií kmene Bacillus Účel, rozsah a princip Postup specifikuje podmínky pro stanovení počtu zárodků kmene Bacillus v krmivech. Stanovení počtu zárodků bakterií kmene Bacillus se provádí anaerobní kultivací na krevním agaru při 37 °C. Počty kolonií, charakteristické pro dané mikroorganismy se vyhodnocují po 18 - 24 hodinách. Opakovatelnost Nestanovena. Reprodukovatelnost Nestanovena.”. |
5. | Mikroprvky | | 5.1. | Stanovení obsahu manganu, zinku, železa a mědi - je uvedeno v příloze 9, část 8 | -A- | 5.2. | Stanovení obsahu kobaltu | -B- | 5.3. | Stanovení obsahu selenu | -B- | 5.4. | Stanovení obsahu jodu | -A- |
6. | Vehikula a pojiva | | 6.1. | Stanovení obsahu oxidu křemičitého je uvedeno v příloze č. 9, část 7 | -A- | 6.2. | Stanovení obsahu oxidu hlinitého je uvedeno v příloze č. 9, část 7 | -A- |
7. | Výpočty | | 7.1. | Vyhodnocování a výpočet výsledků stanovení obsahu doplňkových | | | látek pro difúzní plotnové postupy | -A- |
8. | Antioxidanty | | 8.1. | Stanovení obsahu etoxyquinu | -B- | 8.2. | Stanovení obsahu butylhydroxytoluenu; butylhydroxyanisolu a galátů | -B- |
9. | Barviva | | 9.1. | Stanovení obsahu kapsantinu | -B- | 9.2. | Stanovení obsahu nativních a přidaných karotenoidů | -B- |
10. | Konzervanty | | 10.1. | Stanovení obsahu kyseliny mravenčí | -B- | 10.2. | Stanovení obsahu oxidu siřičitého | -B- | 10.3. | Stanovení obsahu formaldehydu | -A- |
11. | Zchutňovadla | | 11.1. | Stanovení obsahu sacharinu | -B- |
12. | Mikrobiotika | | 12.1. | Stanovení počtu zárodků bakterií kmene Streptococcus | -B- | 12.2. | Stanovení počtu zárodků bakterií kmene Baci11us | -B- |
|
| 30. | V příloze č. 13 „Seznam postupů speciálního zkoušení krmiv”se v tabulce za bod 5. doplňuje bod 6., který zní: 6. | „Mikroskopická identifikace a určování složek živočišného původu Princip Representativní a vhodně upravený vzorek se použije pro identifikaci. Komponenty živočišného původu jsou identifikovány na základě typických, mikroskopicky rozlišitelných charakteristik (např. svalová vlákna a jiné masité části, chrupavky, kosti, rohy, chlupy, štětiny, krev, peří, vaječné skořápky, rybí kosti, šupiny). Identifikace musí být provedena v prosívaných frakcích i v koncentrovaném sedimentu.”. |
|
| 31. | Příloha č. 14 zní: „Příloha č. 14 k vyhlášce č. 222/1996 Sb. Zkoušení homogenity 1. | | Homogenita premixů a krmiv s použitím premixů Zkoušení homogenity se uskutečňuje pomocí doplňkové látky nebo přidané aminokyseliny, dávkované do premixu nebo do krmiv s použitím premixu. Tato doplňková látka nebo aminokyselina musí být stanovitelná metodami zkoušení, které jsou uvedené v přílohách č. 7 až 10. Homogenita se zkouší v rámci jedné partie. | 2 | | Zkoušení homogenity partie Pro test homogenity partie se vybere nj obalů nebo u volně ložených krmiv nj hypotetických částí partie a z každé z nich se odebere jediný dílčí vzorek, který se samostatně upraví a tím se získá nj zkušebních vzorků. Z výsledků zkoušek x1, x2, x3...... xnj se stanoví analýza s2. | 3. | | Stanovení celkového rozptylu Pro stanovení celkového rozptylu použijeme výraz: |
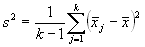
kde: k je celkový počet odebraných dílčích vzorků (počet úrovní) xj je průměr uvnitř úrovně x je průměr ze všech analytických stanovení (celkový průměr), uvedených ve sloupci 3 protokolu o zkouškách 4. | | Stanovení rozptylu metody Pro stanovení rozptylu zkušební metody použijeme výraz: |
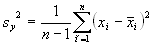
kde: n je počet paralelních opakování pro ověření metody (ověřovací série) xi je i-té stanovení na vzorku, který je použit k ověření metody (ověřovací série), xj je průměr stanovení u vzorku, který je použit k ověření metody (ověřovací série), uvedených ve sloupci 7 protokolu o zkouškách 5. | | Partie krmiva nebo premixu se považuje za homogenní pouze tehdy, když platí: |
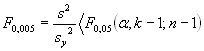
6. | | Počet vzorkovaných obalů nebo hypotetických částí je následující: |
Počet obalů v partii | Vzorkovaná hmotnost volně loženépartie - t | Počet vzorkovaných obalů- částí (díl. vzorků) | do 25 | do 1,50 | 5 | 26 - 50 | od 1,51 - 2,50 | 6 | 51 - 100 | od 2,51- 5,00 | 7 | 101 - 200 | od 5,01 - 10,00 | 9 | 201 - 300 | od 10,01 - 15,00 | 11 | 301 - 500 | od 15,01 - 25,00 | 13 | 501 - 800 | od 25,01 - 40,00 | 16 | 801 - 1 300 | od 40,01 - 65,00 | 20”. |
|