| 6. | Za metodu B.38 se doplňují metody B.39., B.40. a B.41, které znějí: „B.39. TEST NEPLÁNOVANÉ SYNTÉZY DNA V SAVČÍCH JATERNÍCH BUŇKÁCH IN VIVO 1. | METODA Metoda je replikací OECD TG 486, Unscheduled DNA Synthesis (UDS) Test with Mammalian Liver Cells In Vivo (1997). |
1.1 | ÚVOD Účelem testu neplánované syntézy DNA (unscheduled DNA synthesis, UDS) v savčích jaterních buňkách in vivo je určit látky, vyvolávající reparaci DNA v jaterních buňkách pokusných zvířat (1) (2) (3) (4). Tento test in vivo představuje metodu pro zjišťování genotoxických účinků chemických látek v játrech. Výsledek testu indikuje poškození DNA v jaterních buňkách a její následnou reparaci. Játra jsou obvykle hlavním místem metabolismu absorbovaných sloučenin; jsou proto vhodným objektem pro detekci poškození DNA in vivo. Existují-li doklady o tom, že se testovaná látka do cílové tkáně nedostane, není tento test vhodný. Výsledek neplánované syntézy DNA (UDS) se hodnotí tak, že se stanoví absorpce značených nukleosidů v buňkách, které neprocházejí plánovanou (S-fáze) syntézou DNA. Nejběžnější je metoda, při které se autoradiograficky stanoví thymidin značený tritiem (3H-TdR). Pro testy UDS in vivo se nejčastěji používají potkaní játra. Jiné tkáně než játra se sice také mohou použít, nejsou však předmětem této metody. Detekce odpovědi závisí na počtu bází DNA, jež jsou v místě poškození odstraněny a nahrazeny. Proto je metoda UDS zvláště vhodná k detekci látek indukujících „longpatch repair“ (20 - 30 bází), zatímco pro látky indukující „shortpatch repair“ (1 - 3 báze) je méně citlivá. Dále může docházet k mutacím v důsledku neopravení, chybného opravení nebo chybné replikace lézí DNA. Rozsah odpovědi UDS neříká nic o přesnosti procesu reparace. Mimoto je možné, že mutagen bude sice s DNA reagovat, ale poškození DNA není opraveno excizním reparačním procesem. To, že UDS test neposkytuje o mutagenní aktivitě specifické informace, je vyváženo jeho potenciální citlivostí, protože poskytuje výsledek v celém genomu. |
1.2 | DEFINICE Buňky v reparaci: net nuclear grain (NNG) vyšší než určitá, předem stanovená hodnota, kterou zdůvodní laboratoř provádějící test. Net nuclear grains (NNG): kvantitativní míra UDS aktivity buněk při autoradiografických testech UDS, vypočtená jako rozdíl mezi počtem zrn v jádře (NG) a průměrným počtem zrn v cytoplasmě (CG): NNG = NG - CG. Počty NNG se vypočítávají pro jednotlivé buňky a následně přepočítány na buňky v kultuře, v paralelních kulturách apod. Neplánovaná syntéza DNA (unscheduled DNA synthesis, UDS): opravná syntéza DNA po excizi a odstranění úseku DNA obsahujícího oblast poškození vyvolaného chemickou látkou nebo fyzikálním činidlem. |
1.3 | PRINCIP METODY Test UDS v savčích jaterních buňkách in vivo indikuje reparační syntézu DNA po excizi a odstranění segmentu DNA obsahujícího oblast poškození vyvolaného chemickou látkou nebo fyzikálním působením. Test vychází obvykle z inkorporace 3H-TdR do DNA jaterních buněk, charakteristických nízkým počtem buněk v S-fázi buněčného cyklu. Inkorporace 3H-TdR se obvykle stanoví autoradiograficky, protože tato technika není tak náchylná k interferenci s buňkami v S-fázi, jako je např. scintilační metoda. |
1.4.1.1 | Výběr živočišného druhu Běžně se používají potkani, lze ovšem použít jakýkoliv vhodný savčí druh. Používají se běžné laboratorní kmeny mladých zdravých dospělých jedinců. Hmotnostní rozdíly by při zahájení studie měly být minimální a u každého pohlaví nemají přesahovat ± 20 % průměrné hmotnosti. |
1.4.2 | Podmínky chovu Všeobecné podmínky chovu jsou uvedeny ve Všeobecném úvodu v části B. Vlhkost by měla být 50 - 60 %. |
1.4.2.1 | Příprava zvířat Zdraví mladí dospělí jedinci se náhodně rozdělí do kontrolní a experimentální skupiny. Jedinci se jednoznačně označí a po dobu minimálně pěti dní se zvířata aklimatizují v laboratorních podmínkách. Klece je třeba uspořádat tak, aby se minimalizovaly případné vlivy toho, jak a kde jsou klece umístěny. |
1.4.2.2 | Testovaná látka/příprava Je-li testovaná látka v pevném stavu a je-li to možné, látka se před podáním zvířatům rozpustí nebo se připraví její suspenze ve vhodném rozpouštědle nebo vehikulu. Kapalné testované látky se mohou podávat přímo nebo se před podáváním ředí. Je třeba používat čerstvé preparáty, ledaže údaje o stálosti (stabilitě) prokazují, že skladování ji neovlivní. |
1.4.3.1 | Rozpouštědlo / vehikulum Rozpouštědlo / vehikulum v používaných dávkách nesmí vyvolávat toxické účinky a nesmí s testovanou látkou chemicky reagovat. Používá-li se ne příliš známé rozpouštědlo, musí být jeho použití podpořeno údaji o kompatibilitě s testovanou látkou. Doporučuje se, aby kde je to možné, bylo na prvním místě použito vodné rozpouštědlo / vehikulum. |
1.4.3.2 | Kontroly Do každého testu je třeba pro každé pohlaví zařadit souběžné pozitivní a negativní (rozpouštědlo/vehikulum) kontroly. Je třeba zacházet se zvířaty ve všech skupinách stejně. Pozitivní kontroly by měly indukovat UDS při dávkách kdy lze očekávat jejich detekovatelné zvýšení nad spontánní úroveň. Pozitivní kontroly vyžadující metabolickou aktivaci se používají v dávkách vedoucích ke středně vysoké odezvě (4). Dávky při pozitivní kontrole se volí tak, aby byly účinky patrné, ale přitom nenapovídaly hodnotiteli totožnost zakódovaného preparátu. Mezi látky pro pozitivní kontrolu patří například: Doba odběru vzorku | Látka | CAS | EINECS | odběr v intervalu (2 - 4 hodin ) | N-nitrosodimethylamin | 62-75-9 | 200-249-8 | odběr v intervalu (12 - 16 hodin) | N-2-fluorenylacetamid (2-AAF) | 53-96-3 | 200-188-6 |
Je možno použít i jiné vhodné látky. Je možná aplikace pozitivní kontroly jinou cestou, než je podávána testovaná látka. |
1.5.1 | Počet a pohlaví zvířat V každé skupině musí být minimálně tři analyzovatelní jedinci. Pokud existuje historická databáze, pak pro souběžné skupiny negativní a pozitivní kontroly postačují jeden, nebo dva jedinci. Pokud v době, kdy se studie provádí, existují údaje ze studií s týmž živočišným druhem využívajících týž expozičních cest, prokazující, že mezi oběma pohlavími nejsou v toxicitě podstatné rozdíly, je možné provést testování pouze na jednom pohlaví, nejlépe na samcích. Tam, kde humánní expozice testovaným látkám může být pohlavně specifická, jak je tomu například u některých farmaceutických přípravků, provádí se test na zvířatech odpovídajícího pohlaví. |
1.5.2 | Dávkovací schéma Testovaná látka se obvykle podává jednorázově. 1.5.3 Dávkování Obvykle se používají dvě různé dávky. Nejvyšší dávka je definována jako dávka vyvolávající takové známky toxicity, že při vyšší dávce ve stejném režimu by se očekával letální účinek. Nižší dávka představuje obecně 50-25 % dávky vyšší. Látky, jež v nízkých netoxických dávkách vykazují specifickou biologickou aktivitu, jako jsou hormony nebo mitogeny, mohou představovat výjimky z těchto kritérií pro stanovení dávek a vyhodnocují se případ od případu. Provádí-li se studie ke zjištění rozpětí toxicity, protože potřebné údaje nejsou k dispozici, je třeba ji realizovat v téže laboratoři a za použití stejného živočišného druhu, kmene, pohlaví a pokusného režimu, jaké se pak použijí v hlavní studii. Jako nejvyšší dávku lze také definovat dávku vyvolávající určité známky toxicity v játrech (např. pyknotická jádra). |
1.5.4 | Limitní test Jestliže test při dávce minimálně 2 000 mg/kg hmotnosti podané v jedné dávce nebo ve dvou dávkách v jeden den nevyvolává žádné pozorovatelné toxické účinky a jestliže se na základě údajů o strukturně příbuzných látkách neočekává genotoxicita, nemusí se provést úplná studie. Podle očekávané humánní expozice může být použita v limitním testu vyšší dávka. |
1.5.5 | Aplikace látky Testovaná látka se obvykle vpravuje žaludeční sondou. V odůvodněných případech mohou být přijatelné i jiné expoziční cesty. Intraperitoneální aplikace se však nedoporučuje, protože by se tím mohla játra vystavit působení testované látky přímo, nikoli krevním oběhem. Maximální objem kapaliny, která se dá sondou nebo injekcí najednou vpravit, závisí na velikosti pokusného zvířete a nemá překročit 2 ml/100 g hmotnosti organismu; vyšší dávky musí být zdůvodněné. S výjimkou dráždivých nebo žíravých látek, jež normálně vykazují při vyšších koncentracích horší účinky, je třeba upravit koncentrace látky tak, aby objem byl ve všech dávkových úrovních stejný a minimalizovala se tak objemová variabilita. |
1.5.6 | Příprava jaterních buněk Jaterní buňky se z pokusných zvířat zpracovávají obvykle 12 - 16 hodin po podání dávky testované látky. Obvykle je zapotřebí ještě další odběr (obvykle 2 - 4 hodiny po podání látky), ledaže je po 12 - 16 hodinách pozitivní reakce zjevná. Je ovšem možno použít i jiné časy odběru vzorků, je-li to odůvodněné na základě toxokinetických údajů. Krátkodobé kultury savčích jaterních buněk se obvykle zakládají perfuzí jater in situ kolagenázou. Je třeba zajistit, aby se čerstvě disociované jaterní buňky mohly přichytit ke vhodnému povrchu. Jaterní buňky ze zvířat z negativní kontroly mají mít minimálně 50 % životaschopnost (5). |
1.5.7 | Stanovení UDS Čerstvě izolované savčí jaterní buňky se po vhodnou dobu (např. 3 - 8 hodin) obvykle inkubují v médiu obsahujícím 3H-TdR. Po inkubaci se médium odstraní; buňky se potom mohou inkubovat v médiu obsahujícím nadbytek neznačeného thymidinu, aby se snížila neinkorporovaná radioaktivita (tzv. „cold chase“). Buňky se pak promyjí, fixují a vysuší. Při delších inkubačních intervalech nemusí se „cold chase“ provádět. Sklíčka s preparáty se ponoří do autoradiografické emulze, exponují ve tmě (např. po dobu jednoho nebo dvou týdnů v chladničce), vyvolají, obarví a počítají se exponovaná stříbrná zrna. Z každého jedince se připraví dva nebo tři preparáty. |
1.5.8 | Analýza Mikroskopické preparáty musí obsahovat dostatečný počet buněk s normální morfologií, aby bylo možno UDS vyhodnotit. Mikroskopicky se hodnotí zjevné známky cytotoxicity (např. pyknóza, snížená úroveň radioaktivního značení). Preparáty se před počítáním zrn zakódují. Vždy na minimálně dvou preparátech z každého jedince se obvykle hodnotí 100 buněk; pokud je buněk méně než 100 na jednoho jedince, musí to být zdůvodněné. Při počítání zrn se nevyhodnocují jádra v S-fázi, ale podíl buněk v S-fázi se registruje. Vhodnou metodou se stanoví stupeň inkorporace 3H-TdR do jader a cytoplazmy v morfologicky normálních buňkách, zjištěných podle depozice stříbrných zrnek. |
2.1 | ZPRACOVÁNÍ VÝSLEDKŮ Výsledky zahrnují údaje z jednotlivých preparátů a zvířat. Mimoto se všechna data shrnou v tabelární formě. Pro každou buňku, každého jedince a každou dávku a čas se stanoví čistý počet „nuclear grain“ (NNG) odečtením počtu CG od počtu NG. Počítají-li se „buňky v opravě“, musí být kritéria, kterými se tyto buňky určují, zdůvodněna a podložena daty z historických nebo souběžných negativních kontrol. Numerické výsledky se mohou vyhodnotit statistickými metodami; pokud se statistické testy použijí, je třeba je vybrat a zdůvodnit ještě před započetím studie. |
2.2 | VYHODNOCENÍ A INTERPRETACE VÝSLEDKŮ Kritéria pro pozitivní / negativní reakci zahrnují: pozitivní | (I) | hodnoty NNG nad předem stanoveným prahem, zdůvodněným na základě historických dat dané laboratoře | nebo | (II) | hodnoty NNG významně vyšší než u souběžné kontroly | negativní | (I) | hodnoty NNG na úrovni/pod úrovní historického prahu u kontrol | nebo | (II) | hodnoty NNG nejsou signifikantně vyšší než souběžná kontrola |
Je třeba uvážit biologickou významnost získaných dat, což znamená, že je třeba vzít v úvahu parametry, jako jsou variabilita mezi jednotlivými jedinci, vztah dávka-odpověď a cytotoxicita. Při vyhodnocování výsledků lze použít statistické metody; statistická významnost by však neměla být pro pozitivní reakci rozhodujícím faktorem. Většina experimentů poskytuje jednoznačné pozitivní nebo negativní výsledky, v ojedinělých případech však nelze ze získaného souboru dat vyvodit o aktivitě testované látky definitivní závěr. Výsledky mohou být stále nejednoznačné nebo problematické, i když se experiment několikrát opakuje. Pozitivní výsledek testu UDS se savčími jaterními buňkami in vivo ukazuje, že testovaná látka vyvolává v savčích jaterních buňkách in vivo poškození DNA, které lze opravit neplánovanou syntézou DNA in vitro. Negativní výsledek ukazuje, že za daných experimentálních podmínek testovaná látka nevyvolává takové poškození DNA, jež je tímto testem zjistitelná. Je třeba vzít v úvahu, jaká je pravděpodobnost, že testovaná látka dosáhne širokého použití nebo je specifická pro určitou cílovou tkáň (např. systémová toxicita). |
3. | ZÁVĚREČNÁ ZPRÁVA ZPRÁVA O PRŮBĚHU POKUSU Ve zprávě o průběhu pokusu je třeba uvést tyto informace: Rozpouštědlo / vehikulum: |
- | zdůvodnění volby vehikula | - | rozpustnost a stabilita testované látky v rozpouštědle/vehikulu, pokud je známa. |
Pokusná zvířata: - | použitý živočišný druh/kmen, | - | počet, věk a pohlaví jedinců, | - | původ, chovné podmínky, strava apod., | - | hmotnost jednotlivých zvířat na počátku testu, včetně hmotnostního rozpětí, průměrů a směrodatných odchylek pro jednotlivé skupiny. |
Podmínky pokusu: - | pozitivní a negativní (rozpouštědlo/vehikulum) kontroly, | - | údaje ze studie pro určení rozpětí, byla-li provedena, | - | zdůvodnění volby i dávek, | - | podrobnosti o přípravě testované látky, | - | podrobnosti o podávání testované látky, | - | zdůvodnění způsobu podávání, | - | případné metody k ověření, že se látka dostala do krevního oběhu nebo do cílové tkáně, | - | případný převod koncentrace látky v potravě/pitné vodě (ppm) na faktickou dávku (mg/kg hmotnosti /den), | - | podrobnosti o kvalitě potravy a vody, | - | podrobné schéma podávání testované látky a odběru vzorků, | - | metody zjišťování toxicity, | - | metoda přípravy a kultivace jaterních buněk, | - | použitá autoradiografická metoda, | - | počet připravených preparátů a počet hodnocených buněk, | - | kritéria analýzy, | - | kritéria, jimiž se studie hodnotí jako pozitivní, negativní nebo nejednoznačná. Výsledky: |
- | průměrné hodnoty počtů stříbrných zrn v jádrech, cytoplazmě a „net nuclear grains“ pro jednotlivé preparáty, zvířata a skupiny, | - | vztah dávka-odpověď, pokud je k dispozici, | - | statistické hodnocení, bylo-li provedeno, | - | známky toxicity, | - | údaje ze souběžných negativních (rozpouštědlo/vehikulum) a pozitivních kontrol, | - | historické údaje z negativních (rozpouštědlo/vehikulum) a pozitivních kontrol včetně rozpětí, průměrů a směrodatných odchylek, | - | počet „buněk v opravě“, byl-li stanoven, | - | počet buněk v S-fázi, byl-li stanoven, | - | životaschopnost buněk. Diskuse výsledků. Závěry. |
B.40. LEPTAVÉ ÚČINKY NA KŮŽI 1.1 | ÚVOD Evropské centrum pro validizaci alternativních metod (European Centre for the Validation of Alternative Methods, ECVAM, Joint Research Centre, European Commission) schválilo jakožto vědecky validní dva testy in vitro na leptavé účinky na kůži: test na principu měření transkutánního elektrického odporu kůže potkana (transcutaneous electrical resistance, TER) a test využívající modelu lidské kůže. Validizační studie ECVAM prokázala, že oba testy dokáží spolehlivě rozlišovat mezi známými látkami leptajícími a neleptajícími kůži. Mimoto test vycházející z modelu lidské kůže umožňuje správně rozlišovat jednotlivé stupně leptavých účinků (známé látky způsobující těžké poleptání kůže R35, a ostatní látky způsobující poleptání kůže, R34). Je uveden popis a postupy obou testů; výběr mezi oběma testy závisí na konkrétních požadavcích a na preferencích uživatele. |
1.2 | DEFINICE Poleptání kůže: způsobení nevratného poškození tkáně kůže po aplikaci testované látky. |
1.3 | REFERENČNÍ LÁTKY Žádná referenční látka není specifikována, viz však odst. 1.5.3.4 a 1.7.2.3. |
1.4 | PRINCIP METODY - TEST TER NA KŮŽI POTKANA Testovaný materiál se nanese na dobu až 24 hodin na epidermální povrch terčíků kůže odebrané z mladých potkanů utracených humánním způsobem. Látky, které mají leptavé účinky, jsou identifikovány podle své schopnost porušit normální integritu a bariérové funkce stratum corneum. Tato schopnost se měří jakožto pokles inherentního transkutánního elektrického odporu (TER) pod určitou prahovou hodnotu (5 k?) (4) (5). Dráždivé a nedráždivé látky TER pod prahovou hodnotu nesnižují. V případě detergentů a neutrálních organických látek (jejichž definici viz v lit. (6)) je možno do zkušebního postupu zařadit test fixace barviva, aby se snížil počet falešných pozitivních výsledků, jež se u těchto typů chemických látek vyskytují (2) (7). |
1.5 | POPIS METODY - TEST TER NA KŮŽI POTKANA |
1.5.1 | Pokusná zvířata Pro přípravu kožních terčíků jsou používáni mladí (20- až 23-denní) potkani, Wistar nebo srovnatelný kmen. Malými nůžkami na zvířata se pečlivě odstraní srst z dorzální a boční plochy. Zvířata se pak omyjí pečlivým otíráním a oblast se ponoří do roztoku antibiotika, například streptomycinu, penicilinu, chloramfenikolu nebo amfotericinu, v koncentracích inhibujících růst bakterií. Třetí nebo čtvrtý den po prvním omytí se zvířata omyjí antibiotiky znovu a během 3 dní se použijí. Pro přípravu kožních vzorků nesmějí být zvířata starší než 31 dní. |
1.5.2 | Příprava terčíků kůže Zvířata se humánním způsobem usmrtí, sejme se kůže z dorzální plochy a z té se opatrně sloupne přebytečný tuk. Kůže se přiloží přes konec polytetrafluorethylenové (PTFE) trubice, a to epidermální stranou k trubici. Přes konec trubice se přetáhne gumový O-kroužek, kterým se kůže připne, a přebytečná tkáň se odřízne. Rozměry trubice a O-kroužku ukazuje obr. 1. Gumový O-kroužek se pak zatěsní pečlivě ke konci PTFE trubice žlutou vazelínou. Trubice se ponoří do nádoby obsahující roztok síranu hořečnatého (154 mM), kde je přidržována pružinovou sponou (obr. 2). |
1.5.3.1 | Nanesení testované látky Je-li testovaná látka v tekutém stavu, nanese se na epidermální povrch uvnitř trubice (obr. 2). Je-li ve stavu pevném, nanese se na terčík v takovém množství, aby se pokryl celý povrch epidermis, na povrch látky se přidá 150 µl deionizované vody a trubicemi se jemně zatřepe. Testovaná látka musí mít s kůží maximální možný kontakt. U některých pevných látek toho lze dosáhnout zahřátím látky na 30°C, aby se roztavila, nebo rozetřením zrnitého materiálu na jemný prášek. Použijí se vždy tři terčíky pro každou látku. Látka se nanáší na dobu 24 hodin (viz též 1.5.3.4) a odstraní se promýváním proudem vodovodní vody teplé maximálně 30°C tak dlouho, dokud se látka vyplavuje. Odstranění testované látky, která v trubici ztuhla, se dá napomoci vymýváním prudkým proudem vody teplé zhruba 30°C. |
1.5.3.2 | Měření TER Transkutánní elektrický odpor (TER) se měří pomocí nízkonapěťového impedančního můstku pro střídavý proud (např.. AIM 401 nebo 6401 či ekvivalentního). Před měřením elektrického odporu se sníží povrchové napětí kůže přídavkem dostatečného objemu 70% ethanolu, kterým se pokryje epidermis. Po několika sekundách se ethanol odstraní tak, že se trubice otočí, a tkáň se hydratuje přídavkem tří mililitrů 154 mM roztoku síranu hořečnatého. Elektrody můstku se přiloží na obě strany kůže a změří se odpor v k?/terčík (obr. 2). Rozměry elektrod a délku holé elektrody pod krokosvorkou ukazuje obr. 1. Svorka vnitřní (silné) elektrody se během měření uloží navrch PTFE trubice tak, aby byla do roztoku síranu hořečnatého ponořena vždy stejná délka elektrody. Vnější (tenká) elektroda se uloží do receptorové komůrky tak, aby ležela na dně. Je třeba dodržovat konstantní vzdálenost mezi spodní hranou pružinové svorky a spodkem PTFE trubice (obr. 1), tato vzdálenost má vliv na získanou hodnotu odporu. Upozorňujeme, že je-li naměřený odpor vyšší než 20 k?, může to být důsledek toho, že testovaná látka překrývá epidermální povrch terčíku kůže. Je možno se pokusit tento povlak odstranit, například tak, že se PTFE trubice utěsní palcem v rukavici a zhruba 10 sekund se protřepává, roztok síranu hořečnatého se vylije a měření odporu se opakuje s čerstvým roztokem. Průměrná naměřená hodnota TER je akceptována, pokud hodnoty ze souběžné pozitivní a negativní kontroly leží v rozmezích přijatelných pro tuto metodu. Navrhované kontrolní látky a příslušná akceptovatelná rozmezí odporu pro popisovanou metodu a aparaturu jsou tyto: Kontrola | Látka | Rozmezí od oru (k?) | Pozitivní | 10 M kyselina chlorovodíková (36%) | 0,5 - 1,0 | Negativní | destilovaná voda | 10 - 25 |
1.5.3.3 | Modifikovaný postup pro povrchově aktivní látky a neutrální organické látky |
Pokud je při testování povrchově aktivních látek (detergentů) nebo neutrálních organických látek hodnota TER menší nebo rovna 5 k?, lze na této tkáni provést hodnocení průniku (penetrace) barviva. Tímto postupem se zjistí, zda se nejedná o výsledky falešně pozitivní (2). |
| 1.5.3.3.1 Nanesení a odstranění barviva sulforhodaminu B Po prvotním ošetření testovanou látkou se na epidermální povrch všech terčíků nanese na 2 hodiny po 150 µl 10% (w/v) roztoku sulforhodaminu B v destilované vodě. Terčíky kůže se pak zhruba po dobu 10 sekund oplachují prudkým proudem vodovodní vody, která má nejvýše pokojovou teplotu. Tím se má odstranit přebytečné (nenavázané) barvivo. Každý terčík kůže se pak opatrně sejme z PTFE trubice a uloží do nádobky (např. do 20 ml skleněných kyvet pro scintilaci) obsahující 8 ml deionizované vody. Nádobky se po dobu 5 minut jemně třepou, aby se odstranily veškeré zbytky přebytečného (nenavázaného) barviva. Tento oplach se opakuje. Pak se terčíky vyjmou a vloží do nádobek s 5 ml 30 % (w/v) roztoku dodecylsulfátu sodného (SDS) v destilované vodě, kde se přes noc inkubují při teplotě 60°C. Po inkubaci se terčíky vyjmou a zlikvidují a zbývající roztok se odstřeďuje po dobu 8 minut při teplotě 21°C (relativní odstředivá síla 175). Vzorek 1 ml supernatantu se pak zředí 30 % (w/v) roztokem SDS v destilované vodě v objemovém poměru 1 v 5 (v/v) (tj. 1 ml supernatantu + 4 ml roztoku SDS). Optická denzita (OD) roztoku se měří při cca 565 nm. |
1.5 | .3.3 .2 Výpočet obsahu barviva Obsah sulforhodaminu B v terčíku se vypočítá z hodnoty OD (molární extinkční koeficient sulforhodaminu B při 565 nm činí 8,7 . 104; molekulová hmotnost = 580). Obsah sulforhodaminu B se vypočítá pro každý terčík kůže zvlášť a stanoví se průměrná hodnota. Průměrná hodnota navázaného barviva je akceptována za podmínky, že souběžné kontrolní hodnoty spadají do akceptovatelného rozsahu této metody. Za akceptovatelná rozmezí obsahu barviva se u kontrolních látek při této metodě a experimentálním uspořádání považují: Kontrola | Látka | Rozmezí obsahu | | | barviva (µl/ terčík) | Pozitivní | 10 M kyselina chlorovodíková | 40 - 100 | Negativní | destilovaná voda | 15 - 35 |
|
1.5.3.4 | Doplňující informace Je možné zvolit kratší dobu působení testované látky na terčík kůže (např. 2 hodiny) za účelem rozlišení silně leptajících látek. Ve validizační studii však bylo zjištěno, že test TER přeceňuje leptavé schopnosti některých testovaných látek aplikovaných na terčíky kůže na 2 hodiny (2), jakkoliv umožňuje správnou identifikaci leptajících a neleptajících látek po 24-hodinovém působení. Získané hodnoty TER mohou být ovlivněny vlastnostmi a rozměry zkušební aparatury a experimentálním postupem. Prahová hodnota pro leptavé účinky 5 k? byla stanovena na základě údajů získaných na konkrétní aparatuře a při aplikaci postupu uvedeného zde. Pokud by se zkušební podmínky výrazně změnily, mohlo by být třeba použít jiných prahových a kontrolních hodnot. Proto se doporučuje okalibrovat metodiku i prahovou hodnotu otestováním řady referenčních standardů vybraných z látek, jež byly použity při validační studii (3). |
1.6 | PRINCIP ZKUŠEBNÍ METODY - TEST S MODELEM LIDSKÉ KŮŽE Testovaný materiál se nanáší topicky na dobu až 4 hodin na trojrozměrný model lidské kůže, sestávající z rekonstruované epidermis s funkční stratum corneum. Leptající materiál se pozná podle schopnosti vyvolat pokles životnosti buněk stanovené například testem „MTT reduction assay“ (MTT = 3-[4,5-dimetylthiazol-2yl]-2,5 difenyl tetrazolium bromid) pod prahovou hodnotu definovanou pro danou expoziční dobu. Princip testu vychází z předpokladu, že látky způsobující poleptání kůže jsou ty, které dokáží proniknout skrze stratum corneum (difúzí nebo erozí) a jsou dostatečně cytotoxické, aby přivodily smrt buněk v hlubších buněčných vrstvách. |
1.7 | POPIS. METODY - TEST S MODELEM LIDSKÉ KŮŽE |
1.7.1 | Modely lidské kůže Modely lidské kůže mohou pocházet z různých zdrojů, musí však splňovat určitá kritéria. Model musí mít funkční stratum corneum s podkladovou vrstvou živých buněk. Bariérová funkce stratum corneum musí být přiměřeně zachována. To lze prokázat tím, že model bude rezistentní vůči cytotoxicitě po nanesení látek, o nichž je známo, že jsou pro buňky cytotoxické, které však normálně skrze stratum corneum neprocházejí. Model musí za definovaných experimentálních podmínek vykazovat reprodukovatelné výsledky. Životnost živých buněk v modelu musí být dostačující k tomu, aby se dalo dobře rozlišit mezi látkami pozitivní a negativní kontroly. Životnost buněk (měřená například velikostí redukce MTT, tj. OD hodnotou) po expozici látce použité jako negativní kontrola musí ležet v přijatelných mezích pro daný model. Podobně v případě látky pro pozitivní kontrolu (ve srovnání s látkami pro negativní kontrolu) musí hodnoty životnosti spadat do určených mezí. Je velmi důležité, aby bylo prokázáno, že použitý predikční model odpovídá mezinárodnímu validačnímu standardu (2). |
1.7.2.1 | Nanesení testovaného materiálu Je-li testovaná látka tekutá, nanese se tak, aby pokrývala povrch kůže (minimální množství 25 µl/cm2). Je-li pevná, nanese se tak, aby pokrývala kůži, a následně se zvlhčí, aby se s kůží zajistil dobrý styk. Pokud je to třeba, pevné látky se před aplikací roztírají na prášek. U metody nanášení musí být prokázáno, že je vhodná pro široký rozsah látek (2). Po uplynutí doby expozice se materiál z povrchu kůže pečlivě smyje fyziologickým roztokem. |
1.7.2.2 | Měření životnosti buněk K měření životnosti buněk se dá použít jakákoliv validizovaná kvantitativní metoda. Nejčastěji se používá redukce MTT, o které bylo prokázáno že v různých laboratořích poskytuje přesné a reprodukovatelné výsledky (2). Terčík kůže se na dobu 3 hodin ponoří do roztoku MTT o koncentraci 0,3 mg/ml při teplotě 20 - 28°C. Vyloučený modrý formazanový produkt se pak extrahuje (extrakce rozpouštědlem) a koncentrace formazanu se stanoví měřením OD při vlnové délce 545 a 595 nm. |
1.7.2.3 | Doplňující informace Použitý model kůže i přesné dodržení doby působení, promývacího postupu atd. mají na životnost buněk významný vliv. Doporučuje se metodu i predikční model okalibrovat za použití řady referenčních standardů vybraných z látek použitých ve validizační studii ECVAM (3). Je nezbytně nutné, aby bylo prokázáno, že je použitá metoda za použití široké škály látek reprodukovatelná podle mezinárodních standardů jak v rámci dané laboratoře, tak mezi různými laboratořemi. Minimálně musí metoda splňovat kritéria vědecké validity definované dříve (2) a výsledky takové validizační studie musí být zveřejněny ve takovém vědeckém časopise, ve kterém články před zveřejněním procházejí odbornou revizí. |
1.8.1 | Test TER na kůži potkana Hodnoty odporu (v kW) pro testovaný materiál, pozitivní a negativní kontrolu a pro případné standardní referenční látky se uvádějí v tabelární formě, a to data pro všechny replikace a opakované experimenty, průměrné hodnoty a z nich vyvozená klasifikace. |
1.8.2 | Test s modelem lidské kůže Hodnoty OD a vypočtené procento životaschopných buněk se pro testovaný materiál, pozitivní a negativní kontroly a případné standardní referenční látky uvádějí v tabelární formě, a to data pro všechny replikace a opakované experimenty, průměrné hodnoty a z nich vyvozená klasifikace. |
1.9 | VYHODNOCENÍ A INTERPRETACE VÝSLEDKŮ |
1.9.1 | Test TER na kůži potkana Pokud je průměrná hodnota TER pro testovaný materiál vyšší než 5 kW, je látka neleptající. Je-li hodnota TER nižší nebo rovna 5 kW a nejedná se přitom o povrchově aktivní látku (detergent) či neutrální organickou látku, pak testovaná látka leptavé účinky má. U povrchově aktivních látek (detergentů) a neutrálních organických látek, jež poskytují hodnoty TER nepřesahující 5 k?, lze provést zkoušku penetrace barviva. Je-li obsah barviva v terčíku vyšší nebo rovný průměrnému obsahu barviva v terčíku při souběžně provedené pozitivní kontrole s 36 % HCl, je testovaná látka skutečně pozitivní a tedy má leptavé účinky, kdežto je-li obsah barviva v terčíku menší, je testovaná látka falešně pozitivní a tedy leptavé účinky nemá. |
1.9.2 | Test s modelem lidské kůže Hodnota OD pro negativní kontrolu představuje 100 % životaschopnost buněk. Z hodnot OD pro jednotlivé zkušební vzorky se vypočte procentuální životnost vůči negativní kontrole. Hraniční procentický podíl životaschopných buněk, který odděluje látky, které nezpůsobují poleptání kůže, od těch, které poleptání způsobují, respektive odlišuje jednotlivé třídy leptavých vlastností, musí být v predikčním modelu jasně definován předtím, než je metoda validována, a následnou validační studií se musí prokázat, že je tato hraniční hodnota odpovídající. |
3. | ZÁVĚREČNÁ ZPRÁVA ZPRÁVA O PRŮBĚHU POKUSU Ve zprávě o průběhu pokusu je třeba uvést tyto informace: Testovaná látka: |
- | identifikační údaje, fyzikální stav, popřípadě fyzikálně-chemické vlastnosti; pokud se používají referenční látky, uvedou se tyto údaje i pro ně. Podmínky pokusu: |
- | podrobný popis použitého postupu, | - | popis a zdůvodnění všech případných modifikací. Výsledky: |
- | tabulka hodnot odporu (test TER) nebo procentuální podíl životaschopných buněk (test s modelem lidské kůže) pro testovaný materiál, pozitivní a negativní kontroly a případné standardní referenční látky, a to údaje pro všechny replikace resp. opakované experimenty a průměrné hodnoty; | - | popis všech jiných pozorovaných efektů. Diskuse výsledků. Závěry. Obrázek 1 Rozměry PTFE trubice 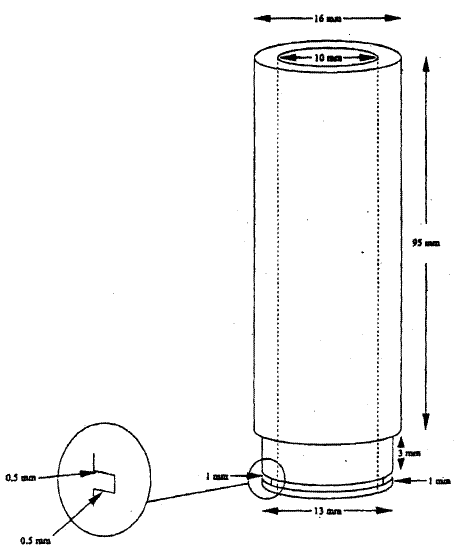
rozměry elektrod 
Obrázek 2 Aparatura pro test TER s kůží potkana 
B.41. FOTOTOXICITA - TEST FOTOTOXICITY 3T3 NRU IN VITRO |
1.1 | ÚVOD Fototoxicita je definována jako toxická odezva (reakce), k níž dochází, je-li kůže poprvé vystavena určitým chemickým látkám a následně pak světlu, nebo je-li podobně kůže ozářena po celkovém podání určité látky. Informace získané v rámci testu fototoxicity 3T3 NRU in vitro slouží ke stanovení fototoxického potenciálu dané testované látky, tedy ke zjištění, zda daná látka ve spojení s expozicí ultrafialovému a viditelnému záření představuje možné nebezpečí nebo nikoli. Toxikologickým výsledkem testu in vitro je stanovení fototoxicity vyvolané kombinovaným působením látky a světla, tímto testem je možné zjistit sloučeniny, které jsou fototoxické in vivo po celkové aplikaci a distribuci v kůži, a sloučeniny, jež působí jako fotoiritanty po topickém nanesení na pokožku. Test fototoxicity 3T3 NRU in vitro byl vypracován a validován v rámci společného projektu EU/COLIPA z let 1992 - 1997 (1) (2) (3) jakožto validní alternativa in vitro vůči různým používaným testům in vivo. V roce 1996 doporučila pracovní schůze OECD přístup následných in vitro testů pro hodnocení fototoxicity (4). Výsledky testu fototoxicity 3T3 NRU in vitro byly porovnány s akutními účinky fototoxicity/fotoiritace in vivo u zvířat a lidí a bylo zjištěno, že tento test má pro uvedené účinky vynikající predikční schopnosti. Test není navržen k tomu, aby předpovídal jiné nepříznivé účinky, jež mohou z kombinovaného působení látky a světla vzniknout, jako je fotogenotoxicita, fotoalergie nebo fotokarcinogenita, i když řada látek tyto specifické vlastnosti vykazuje, reaguje při testu fototoxicity 3T3 NRU in vitro pozitivně. Test není rovněž uspořádán tak, aby umožňoval hodnocení stupně fototoxicity. Sekvenční přístup testování fototoxicity u chemických látek je přiložen viz dodatek. |
1.2 | DEFINICE Iradiance: intenzita ultrafialového (UV) či viditelného záření dopadajícího na povrch; měřená ve W/m2 nebo v mW/cm2. Dávka světla: množství (= intenzita x čas) ultrafialového (UV) nebo viditelného (VIS) záření dopadajícího na povrch, vyjádřené v joulech (= W x s) na jednotku povrchu, např. J/m2 nebo J/cm2. Pásma vlnových délek ultrafialového světla: podle doporučení CIE (Commission International de L'Eclairage) se používá označení UVA (315 - 400 nm), UVB (280 - 315 nm) a UVC (100 - 280 nm). Používají se i jiná vymezení: za hranici mezi pásmy UVA a UVB se často považuje 320 nm a UVA se někdy dělí na UV-A1 a UV-A2 s hranicí zhruba u 340 nm. Životaschopnost (viabilita) buněk: parametr, kterým se měří celková aktivita buněčné populace (např. příjem barviva indikujícího živou buňku, neutrální červeně, do buněčných lysozomů), jež podle parametrů měřených daným testem a jeho uspořádání koreluje s celkovým počtem resp. životností (vitalitou) buněk. Relativní životaschopnost (viabilita) buněk: životaschopnost buněk vyjádřená v porovnání s negativními kontrolami (rozpouštědlo), které prošly celou procedurou testu (buď +UV nebo -UV), ovšem bez působení testované látky. Predikční model: algoritmus, kterým se výsledky testu toxicity transformují do predikce toxického potenciálu. V tomto metodickém návodu pro test je možno k transformaci výsledků testu na fototoxicitu 3T3 NRU in vitro k predikci fototoxického potenciálu použít veličin PIF a MPE. PIF (photo irritation factor, fotoiritační faktor): koeficient představující poměr dvou stejně účinných cytotoxických koncentrací (EC50) testované látky získaných v nepřítomnosti (-UV) a v přítomnosti (+UV) necytotoxického UVA/VIS ozáření. MPE (mean photo effect, střední fotoefekt): nová míra odvozená z matematické analýzy kompletního průběhu dvou křivek koncentrace-odezva získaných v nepřítomnosti (-UV) a v přítomnosti (+UV) necytotoxického UVA/VIS ozáření. Fototoxicita: akutní toxická reakce (odezva), která vzniká po první expozici kůže určité látce a následné expozici kůže světlu, nebo reakce která je obdobně navozena ozářením kůže po systémovém podání určité látky. Fotoiritace: nižší úroveň pojmu „fototoxicita“, týkající se pouze těch fototoxických reakcí, k nimž dochází v kůži poté, co na ni působí (topicky nebo orálně přijatá) nějaká látka. Tyto fototoxické reakce vedou vždy k nespecifickému poškození buněk (reakce podobné jako při nadměrném slunění). Fotoalergie: získaná imunologická reaktivita, která se při prvním působení látky a světla neprojevuje, a kdy je zapotřebí jednotýdenní až dvoutýdenní indukční periody k tomu, aby se reaktivita kůže projevila. Fotogenotoxicita: genotoxická reakce (odezva) s genetickými projevy, ke které dochází poté, co byly buňky vystaveny negenotoxické dávce UV/VIS záření a negenotoxické látky. Fotokarcinogenita: karcinogenita vyvolaná opakovanou aplikací světla a látky. Pokud je tumorogeneze vyvolaná UV zářením zesílena látkou, mluvíme o fotokokarcinogenitě. |
1.3 | REFERENČNÍ LÁTKY Vedle chlorpromazinu jako látky pro pozitivní kontrolu, která je souběžně testována při každé studii, se pro zavedení testu na fototoxicitu 3T3 NRU doporučuje použít jako referenční látky podsoubor z látek, které byly použity při mezilaboratorním porovnávání tohoto testu (1) (3) (13). |
1.4 | PRVOTNÍ ÚVAHY Fototoxické účinky byly pozorovány u řady látek (5) (6) (7) (8), jejichž jediným společným rysem je to, že dokáží absorbovat světelnou energii v oblasti slunečního záření. Podle prvního zákona fotochemie (Grotthausův-Draperův zákon) vyžaduje každá fotoreakce dostatečnou absorpci světelných kvant. Proto by se předtím, než se začne uvažovat o biologickém testování podle tohoto metodického návodu, mělo by se vždy stanovit absorpční spektrum testované látky v UV/VIS oblasti (například podle zkušební metody OECD č. 101). Pokud je molární extinkční/absorpční koeficient nižší než 10 litrů x mol-1 x cm-1, nemá látka fotoreaktivní potenciál a není třeba ji na škodlivé fotochemické účinky testovat ani testem na fototoxicitu 3T3 NRU in vitro, ani žádným jiným biologickým testem (viz dodatek). |
1.5 | PRINCIP METODY Byly zjištěny čtyři mechanismy, kterými může absorpce světla (chemickým) chromoforem vyústit ve fototoxickou reakci (7), přičemž všechny vedou k poškození buněk. Proto je test fototoxicity 3T3 NRU in vitro založen na porovnání cytotoxicity látky testované v přítomnosti a nepřítomnosti necytotoxické dávky UVA/VIS záření. Cytotoxicita se při tomto testu vyjadřuje jako koncentračně závislý pokles příjmu vitálního barviva, neutrální červeně (neutral red, NR) {9), 24 hodin po působení testované látky a ozařování. Buňky Balb/c 3T3 se kultivují po dobu 24 hodin tak, aby se vytvořila kultura buněk v jedné vrstvě (monolayer). Pro každou testovanou látku se preinkubují dvě destičky po 96 jamkách s látkou v osmi různých koncentracích po dobu 1 hodiny. Jedna z obou destiček se pak vystaví necytotoxickému UVA/VIS záření v dávce 5 J/cm2 UVA (+UV experiment), druhá destička se uchovává v temnu (-UV experiment). V obou destičkách se pak médium nahradí médiem kultivačním a po dalších 24 hodinách kultivace se pomocí inkorporace neutrální červeně (neutral red uptake, NRU) po dobu 3 hodin stanoví životaschopnost buněk. Pro každou z osmi koncentrací se stanoví relativní životaschopnost buněk, vyjádřená jako procento hodnot u negativních kontrol. K posouzení fototoxického potenciálu se porovnají koncentračně závislé reakce získané v přítomnosti (+UV) a v nepřítomnosti (-UV) záření, obvykle na úrovni EC50, tj. při koncentraci inhibující životaschopnost buněk o 50 % v porovnání s kontrolami bez ovlivnění. |
1.6 | KRITÉRIA JAKOSTI Citlivost buněk vůči záření UVA, historické údaje: u buněk je třeba pravidelně provádět kontrolu citlivosti vůči záření UVA. Buňky se nasadí v hustotě, která se používá při testu fototoxicity 3T3 NRU in vitro, příští den se vystaví záření UVA v dávce 1 - 9 J/cm2 a další den se testem NRU stanoví životaschopnost buněk. Buňky splňují kritéria jakosti, jestliže jejich životaschopnost po ozáření dávkou UVA záření 5 J/cm2 není nižší než 80 % životaschopnosti kontrolních vzorků uchovávaných v temnu. Při nejvyšší dávce UVA záření 9 J/cm2 nemá být životaschopnost nižší než 50 % životaschopnosti vzorků uchovávaných v temnu. Tato kontrola se provádí zhruba po každé desáté pasáži buněk. Citlivost buněk negativní kontroly vůči záření UVA, běžný test: test splňuje kritéria jakosti, jestliže negativní kontroly (buňky v Earlově vyváženém solném roztoku [Earl's balanced salt solution, EBSS] s 1 % roztokem dimethylsulfoxidu (DMSO) nebo ethanolu (EtOH) nebo bez nich vykazují v experimentu (+UVA) životaschopnost minimálně 80 % v porovnání s neozářenými buňkami v témž rozpouštědle v rámci souběžného experimentu v temnu (-UVA). Životaschopnost negativních kontrol: absolutní optická hustota (OD540 NRU) měřená v NR extraktu negativních kontrol ukazuje, zda oněch 1 x 104 buněk nasazených v každé jamce rostlo během dvou dnů testu s normální dobou zdvojnásobení. Test splňuje kritéria akceptovatelnosti, je-li průměrná hodnota OD540 NRU u kontrol bez ovlivnění větší nebo rovna 0,2. Pozitivní kontrola: při každém testu na fototoxicitu 3T3 NRU in vitro je třeba provést souběžný test se známou fototoxickou látkou. Při validační studii EU/COLIPA byl jako látka pro pozitivní kontrolu použit chlorpromazin (CPZ); proto se tato látka doporučuje. Pro CPZ testovaný dle standardního protokolu v testu fototoxicity 3T3 NRU in vitro byla definována tato kritéria akceptovatelnosti: CPZ ozářený (+UVA): EC50 = 0,1 - 2,0 µg/ml, CPZ neozářený (-UVA): EC50 = 7,0 - 90,0 µg/ml. Fotoiritační faktor (PIF), tzn. posun hodnoty EC50, má být minimálně 6. Místo CPZ se pro souběžnou pozitivní kontrolu dají použít i jiné známé fototoxické látky, pokud jsou vhodné pro charakteristiku chemické skupiny nebo rozpustnosti testované (hodnocené) látky. V takovém případě je třeba na základě historických dat adekvátně definovat jako kritéria akceptovatelnosti rozsahy hodnot EC50 a PIF nebo MPE (střední fotoefekt). |
1.7.1.1 | Buňky Při validační studii byla použita stabilizovaná buněčná linie myších fibroblastů Balb/c 3T3 klon 31, a to buď z ATCC nebo z ECACC; ta se proto doporučuje. Podle stejného protokolu se dají s úspěchem použít i jiné buňky nebo buněčné linie, pokud se kultivační podmínky upraví podle jejich specifických potřeb; je však třeba prokázat, že jsou stejně vhodné. U buněk je třeba pravidelně kontrolovat, že nejsou kontaminovány mykoplazmaty, a smí se použít jen v případě, že je výsledek kontroly uspokojivý. Jelikož citlivost buněk vůči UVA záření může s počtem pasáží narůstat, je třeba používat buňky Balb/c 3T3 z pasáže s nejnižším číslem, pokud možno nižším než 100. Citlivost buněk Balb/c 3T3 vůči UVA záření je třeba pravidelně kontrolovat, a to postupem kontroly jakosti popsaným v tomto metodickém návodu. |
1.7.1.2 | Média a kultivační podmínky Pro rutinní pasážování buněk a během postupu je třeba používat vhodná kultivační média a inkubační podmínky. V případě buněk Balb/c 3T3 se jedná o DMEM obohacený 10 % séra novorozených telat, 4 mM glutaminu, penicilinem a streptomycinem a o inkubaci ve vlhkém prostředí při teplotě 37°C / 7,5 % CO2. Je nezbytné, aby podmínky kultivace zajišťovaly buněčný cyklus v normálním historickém rozmezí pro dané buňky resp. buněčnou linii. |
1.7.1.3 | Příprava kultur Buňky ze zmražených zásobních kultur se nasadí v příslušné hustotě v kultivačním médiu a minimálně jednou se před použitím v testu na fototoxicitu 3T3 NRU in vitro pasážují. Pro test fototoxicity se buňky nasadí v kultivačním médiu v takové hustotě, aby na konci testu (tj. kdy se stanovuje životaschopnost buněk 48 hodin po nasazení) nedošlo ke konfluenci (ke splynutí v souvislou, jednolitou vrstvu buněk). V případě buněk Balb/c 3T3 kultivovaných v destičkách s 96 jamkami se doporučuje hustota 1 x 104 buněk v jedné jamce. Pro každou testovanou látku se buňky nasazují identicky na dvě destičky s 96 jamkami, které pak procházejí celým postupem za identických kultivačních podmínek, s výjimkou doby, kdy je jedna z destiček ozařována (+UVA/VIS) a druhá je uchovávána v temnu (-UVA/VIS). |
1.7.1.4 | Metabolická aktivace Zatímco při všech testech in vitro pro posouzení genotoxického nebo karcinogenního potenciálu je obecným požadavkem použití metabolizujícího systému, není v případě fototoxikologie známa žádná látka, kde by k tomu, aby působila jako fototoxin in vivo nebo in vitro, bylo metabolické transformace zapotřebí. Nepokládá se proto ani za nutné, ani za vědecky odůvodněné, aby se tento test prováděl s nějakým metabolickým aktivačním systémem. |
1.7.1.5 | Testovaná látka / příprava Testovaná látka musí být před použitím čerstvě připravena, ledaže údaje o její stabilitě prokazují, že se dá skladovat. Pokud je pravděpodobné, že by došlo k fotodegradaci, musí se příprava provádět pod červeným světlem. Látka se rozpustí v pufrovaném solném roztoku, například v Earlově vyváženém solném roztoku (EBSS) nebo ve fyziologickém roztoku pufrovaném fosfátem (phosphate buffered saline, PBS), který - aby nemohlo dojít k interferenci během ozařování - nesmí obsahovat žádné proteinové složky ani barevné indikátory pH, pohlcující světlo. Pokud je testovaná látka ve vodě omezeně rozpustná, rozpustí se ve vhodném rozpouštědle v koncentraci stonásobně vyšší, než je požadovaná konečná koncentrace, a následně se zředí v poměru 1 : 100 pufrovaným solným roztokem. Pokud se používá rozpouštědlo, musí být přítomno v konstantním objemu 1 % (v/v) ve všech kulturách, tj. ve všech koncentracích testované látky i v negativních kontrolách. Jako rozpouštědlo se doporučuje dimethylsulfoxid (DMSO) nebo ethanol (EtOH). Vhodná mohou být i další rozpouštědla s nízkou cytotoxicitou, například aceton, je však třeba vždy pečlivě zvážit jejich specifické vlastnosti, jako je případná reakce s testovanou látkou, potlačení fototoxického efektu nebo vychytávání radikálů. Aby se napomohlo rozpouštění, dá se použít míchání resp. sonifikace, popřípadě ohřev na 37 °C |
1.7.1.6 | Ozařování UV světlem / příprava Světelný zdroj: volba správného světelného zdroje a správná filtrace je při testování fototoxicity klíčovým faktorem. Záření v UVA a ve viditelné oblasti je obvykle spojováno s fotosenzibilizací (7) (10), kdežto záření UVB je v tomto směru méně relevantní, je přímo vysoce cytotoxické, přičemž jeho cytotoxicita se při přechodu od 313 nm k 280 nm zvyšuje tisícinásobně. Mezi kritéria pro volbu světelného zdroje patří zásadní požadavek, aby emitoval vlnové délky, jež testovaná látka absorbuje, a aby byla světelná dávka (dosažitelná za přiměřenou dobu) postačující ke zjištění známých fotosenzibilizujících látek. Dále nesmějí být použité vlnové délky a dávky nepatřičně poškozující testovací systém - patří sem i vyzařování tepla (infračervená oblast). Za optimální světelný zdroj se pokládají solární simulátory, jimiž se simuluje sluneční záření. Jako tyto simulátory se používají xenonové výbojky a dále (vysokotlaké) rtuťové halogenové výbojky - ty mají tu výhodu, že vyzařují méně tepla a jsou levnější, sluneční světlo však imitují hůře. Jelikož všechny solární simulátory emitují významné množství záření UVB, je třeba záření filtrovat tak, aby se toto vysoce cytotoxické záření dostatečně zeslabilo. Pro test na fototoxicitu 3T3 NRU in vitro je třeba použít spektrum záření, kde se složka UVB prakticky nevyskytuje (UVA:UVB 20 : 1). Příklad spektrálního rozložení filtrovaného záření solárního simulátoru použitého při validační studii testu na fototoxicitu 3T3 NRU in vitro je v práci (3). Dozimetrie: intenzita světla (iradiance) se musí pravidelně před každým testem fototoxicity kontrolovat pomocí vhodného širokopásmového UV-metru, který musí být kalibrován pro daný zdroj. Funkčnost UV-metru je třeba kontrolovat, k čemuž se doporučuje použít druhý, referenční UV-metr téhož typu a kalibrace. Ideální je, když se v delších intervalech měří spektrální iradiance filtrovaného světelného zdroje a kontroluje se kalibrace širokopásmového UV-metru pomocí spektroradiometru; taková instrumentace ovšem vyžaduje kvalifikovanou obsluhu vyškoleného personálu. Při validační studii bylo zjištěno, že dávka UVA záření 5 J/cm2 je pro buňky Balb/c 3T3 necytotoxická a přitom dostatečně silná, aby excitovala i slabě fototoxické látky. Aby se této dávky dosáhlo během 50 minut, musí být iradiance nastavena na 1,666 mW/cm2. Použije-li se jiná buněčná linie nebo jiný zdroj světla, musí se dávka záření UVA upravit tak, aby buňky nepoškozovala a byla dostatečná k průkazu standardních fototoxinů. Doba světelné expozice se vypočítává podle vzorce: t (min) =  (1 J = 1 W s) (1 J = 1 W s) 1.7.2 Podmínky testu Maximální koncentrace testované látky nemá převýšit hodnotu 100 µg/ml, neboť všechny fototoxické látky byly detekovány při koncentracích nižších, při vyšších koncentracích se zvyšuje četnost falešně pozitivních výsledků (13). Hodnota pH při nejvyšší koncentraci testované látky musí být přijatelná (oblast pH 6,5 - 7,8). Rozsah koncentrací testované látky při použití světla (+UVA) a bez něj (-UVA) je třeba stanovit v rámci předběžných experimentů. Rozsah a postup koncentrační řady se zvolí tak, aby křivky závislosti koncentrace-odezva byly dostatečně podloženy experimentálními údaji. Používá se koncentrační geometrická řada (s konstantním faktorem ředění). |
1.7.3.1 | První den Připraví se suspenze 1 x 105 buněk/ml v kultivačním médiu. Do periferních jamek 96 jamkové mikrotitrační destičky pro tkáňové kultury se odpipetuje po 100 µl samotného média (= slepý pokus), do ostatních jamek se dávkuje po 100 µl buněčné suspenze o denzitě 1 x 105 buněk/ml (=1 x 104 buněk na jamku). Pro každou testovanou látku se připraví dvě destičky - jedna pro stanovení cytotoxicity (-UVA), druhá pro stanovení fotocytotoxicity (+UVA). Buňky se inkubují po dobu 24 hodin (7,5 % CO2, 37 °C), aby se vytvořil semikonfluentní monolayer. Tato inkubační doba umožňuje regeneraci a adherenci buněk a jejich exponenciální růst. |
1.7.3.2 | Druhý den Po inkubaci se kultivační médium z buněk odstraní a promyje dvakrát objemem 150 µl EBSS/PBS na každou jamku. Přidá se 100 µl EBSS/PBS obsahujícího testovanou látku v příslušné koncentraci nebo jenom rozpouštědlo (negativní kontrola). Testovaná látka se přidává v osmi koncentracích. Buňky s testovanou látkou se inkubují v temnu po dobu 60 minut (7,5 % CO2, 37 °C). Část testu s UVA (+UVA) se provádí tak, že se buňky za pokojové teploty ozařují po dobu 50 minut skrz víčko destičky s 96 jamkami zářením UVA o intenzitě 1,7 mW/cm2 (= dávka 5 /cm2). Aby nedocházelo ke kondenzaci vody pod víčkem, je třeba použít ventilátoru. Duplicitní destičky (-UVA) se po dobu 50 minut (= expoziční doba UVA) uchovávají za pokojové teploty v temném boxu. Roztok se odstraní a jamky se promyjí dvakrát 150 µl EBSS/PBS. Poté se naplní kultivačním médiem a přes noc (18 - 22 hodin) se inkubují (7,5 % CO2, 37 °C). |
1.7.3.3 | Třetí den Mikroskopické hodnocení Buňky se prohlédnou pod mikroskopem s fázovým kontrastem. Zaznamenají se změny morfologie buněk způsobené cytotoxickým účinkem testované látky. Tato kontrola se doporučuje, aby se eliminovaly experimentální chyby, ale při vyhodnocování cytotoxicity nebo fototoxicity se tyto záznamy nepoužijí. Test příjmu neutrální červeně (NR) Buňky se promyjí objemem 150 µl předehřátého EBSS/PBS. Promývací roztok se odstraní jemným poklepem. Přidá se 100 µl média s NR a inkubuje se při 37 °C ve zvlhčené atmosféře s 7,5 % CO2 po dobu 3 hodin. Po inkubaci se médium s NR odstraní a buňky se promyjí objemem 150 µl EBSS/PBS, jenž se pak zcela a důkladně odstraní (je také možno destičky zcentrifugovat v obrácené poloze). Přidá se přesně 150 µl roztoku na uvolnění NR (čerstvě připravená směs ethanol/ kyselina octová). Mikrotitrační destičky se po dobu 10 minut rychle třepou na třepačce, dokud se NR z buněk nevyextrahuje a nevytvoří se homogenní roztok. Na spektrofotometru se změří optická hustota extraktu NR při 540 nm za použití slepého pokusu jako srovnávacího roztoku. Údaje se uchovají ve vhodném formátu (např. ASCII) pro další analýzu. |
1.8 | KVALITA A KVANTITA ÚDAJŮ Údaje musí umožňovat smysluplnou analýzu vztahu koncentrace-odezva při aplikaci UVA/VIS záření a bez ní. Je-li zjištěna cytotoxicita, koncentrační rozsah a postup jednotlivých koncentrací se nastaví tak, aby se experimentální údaje daly vyjádřit křivkou. Jelikož testovaná látka může být až do definované limitní koncentrace 100 µg/ml v experimentu ve tmě (-UVA) necytotoxická, ale při ozařování (+UVA) vysoce cytotoxická, může dojít k tomu, že se koncentrační rozsahy v obou částech experimentu budou muset řádově lišit, aby byl splněn požadavek adekvátní kvality dat. Pokud není cytotoxicita zjištěna v žádné z obou částí experimentu (ani při -UVA, ani při +UVA), postačuje testování s velkým rozestupem mezi jednotlivými dávkami až do nejvyšší koncentrace. Jsou-li výsledky hraniční - blízko dělicí čáry predikčního modelu - je třeba test pro ověření opakovat. Považuje-li se opakování testu za potřebné, může být důležité pozměnit experimentální podmínky, aby se dosáhlo jasného výsledku. Klíčovou proměnnou v tomto testu je příprava roztoků testované látky, nejvhodnější při jeho opakování je variace těchto podmínek (spolurozpouštědlo, triturace, sonifikace). Lze také uvažovat o změnách inkubační doby před ozařováním. U látek, jež jsou ve vodě nestálé, může mít významný vliv zkrácení doby. |
1.9 | ZPRACOVÁNÍ VÝSLEDKŮ Pokud je to možné, stanoví se koncentrace testované látky vedoucí k 50 % inhibici buněčného příjmu NR (EC50). To lze učinit tak, že se na data koncentrace-odezva použije jakákoliv vhodná metoda nelineární regrese (nejlépe Hillova funkce nebo logistická regrese) nebo se použije jiná vhodná metoda proložení (14). Než se hodnota EC50 použije pro další výpočty, je třeba zkontrolovat kvalitu proložení. K výpočtu hodnoty EC50 je také možno použít grafické metody. V tomto případě se doporučuje použít pravděpodobnostní papír (osa x: log, osa y: probit), protože po této transformaci bývá křivka koncentrace-odezva mnohdy téměř lineární. |
1.10 | VYHODNOCENÍ VÝSLEDKŮ (PREDIKČNÍ MODELY) |
1.10.1 | Predikční model, verze 1: fotoiritační faktor (PIF) Pokud se získají úplné křivky koncentrace-odezva jak za přítomnosti (+UVA), tak za nepřítomnosti (-UVA) světla, se fotoiritační faktor (PIF) vypočítá podle vzorce (a) PIF =  PIF < 5, nepředpovídá žádný fototoxický potenciál, kdežto PIF > 5 fototoxický potenciál předpovídá. Je-li látka cytotoxická pouze při +UVA, kdežto při -UVA je necytotoxická, nedá se PIF vypočítat, i když se jedná o výsledek, který indikuje, že látka má fototoxický potenciál. V takovém případě se dá vypočítat tzv. „> PIE“, když se test cytotoxicity (-UV) provede až po maximální zkušební koncentraci (Cmax) a tato hodnota se dosadí do vzorce: (b) >PIF =  Pokud se dá vypočítat pouze „>PIF“, pak každá hodnota > 1 předpovídá fototoxický potenciál. Jestliže se nedá vypočítat ani EC50 (-UV), ani EC50 (+UV), protože látka nevykazuje cytotoxicitu až do nejvyšší zkušební koncentrace, je to indikací toho, že látka nemá žádný fototoxický potenciál. V takovém případě se používá formální „PIF = * 1“, čímž se charakterizuje výsledek (c) PIF =* 1 = Pokud se dá získat pouze hodnota „PIF = * 1“, předpovídá to, že není přítomen žádný fototoxický potenciál. V případech (b) a (c) je třeba při predikci fototoxického potenciálu vzít bedlivě v úvahu koncentrace, jichž se při testu dosáhlo. |
1.10.2 | Predikční model, verze 2: střední fotoefekt (MPE) Je možno také použít novější verze modelu pro predikci fototoxického potenciálu, vypracovaného za použití dat z validační studie EU/COLIPA (15) a odzkoušeného za podmínek slepé studie stanovení fototoxicity in vitro u látek UV filtrů (13). V tomto modelu jsou překonána omezení modelu PIF v těch případech, kde nelze získat hodnotu EC50. V tomto modelu se používá veličina „střední fotoefekt“ (MPE) založená na porovnání celého průběhu křivek koncentrace-odezva. Pro aplikaci modelu MPE byl na Humboldtově univerzitě v Berlíně vyvinut speciální počítačový software, který lze obdržet zdarma. |
1.11 | INTERPRETACE VÝSLEDKŮ Pozitivní výsledek testu (PIF > 5 nebo MPE > 0,1) ukazuje, že daná látka má fototoxický potenciál. Pokud se k tomuto výsledku dojde při koncentracích nižších než 10 µg/ml, je pravděpodobné, že látka bude působit jako fototoxin také za různých expozičních podmínek in vivo. Získá-li se pozitivní výsledek pouze při nejvyšší zkušební koncentraci (100 µg/ml), bude pro posouzení nebezpečnosti nebo fototoxické schopnosti dané látky nejspíše zapotřebí dalších informací. Sem mohou spadat informace o penetraci, absorpci a možné akumulaci látky v kůži, nebo údaje z testování dané látky v jiném potvrzujícím alternativním testu, například za použití modelu lidské kůže in vitro. Negativní výsledek testu fototoxicity 3T3 NRU in vitro (PIF < 5 nebo MPE < 0,1 ) ukazuje, že testovaná látka není fototoxická pro použité savčí buňky v daných podmínkách. V případech, kdy by se látka dala testovat i při nejvyšší koncentraci 100 µg/ml, negativní výsledek znamená, že látka nemá žádný fototoxický potenciál a fototoxicita in vivo se dá považovat za nepravděpodobnou. V případech, kdy byly při nižších koncentracích získány identické koncentrační závislosti toxické reakce (EC50 +UV a EC50 -UV), je interpretace dat stejná. Naproti tomu pokud nebyla prokázána žádná toxicita (+UV ani -UV) a pro omezenou rozpustnost látky se nedalo dosáhnout koncentrace 100 µg/ml, je možno považovat tento test pro danou látku za ne zcela vhodný a mělo by se uvažovat o jiném, potvrzujícím testu (například s použitím modelu kůže in vitro nebo modelu kůže ex vivo nebo test in vivo). |
3. | ZÁVĚREČNÁ ZPRÁVA ZPRÁVA O PRŮBĚHU POKUSU Ve zprávě o průběhu pokusu je třeba uvést tyto informace: Testovaná látka: |
- | identifikační údaje a číslo CAS, je-li známo, | - | fyzikální povaha a čistota, | - | fyzikálně-chemické vlastnosti, jež jsou k provedení testu důležité, | - | stabilita a fotostabilita, jsou-li známy. Rozpouštědlo: |
- | zdůvodnění volby daného rozpouštědla, | - | rozpustnost testované látky v tomto rozpouštědle, | - | procentický podíl rozpouštědla v působícím médiu (EBSS nebo PBS). Buňky: |
- | typ a zdroj buněk, | - | nepřítomnost mykoplazmat, | - | číslo buněčné pasáže, je-li známo, | - | citlivost buněk vůči záření UVA stanovená pomocí ozařovacího zařízení, jež se v testu na fototoxicitu 3T NRU in vitro používá. Podmínky pokusu (a) - inkubace před ovlivněním a po něm: |
- | typ a složení kultivačního média, | - | podmínky inkubace (koncentrace CO2, teplota, vlhkost), | - | doba inkubace (zpracování před ní a po ní)., Podmínky pokusu (b) -ovlivnění látkou: |
- | zdůvodnění volby koncentrací testované látky, které se použijí v přítomnosti ozařování UV/VIS zářením a bez něj, | - | v případě omezené rozpustnosti testované látky a absence cytotoxicity zdůvodnění nejvyšší testované koncentrace, | - | typ a složení působícího média (pufrovaný solný roztok), | - | doba ovlivňování látkou. Podmínky pokusu (c) - ozařování: |
- | zdůvodnění volby daného světleného zdroje, | - | spektrální charakteristika záření světelného zdroje, | - | charakteristiky propustnosti/absorpce použitého filtru (filtrů), | - | charakteristika radiometru a podrobnosti o jeho kalibraci, | - | vzdálenost světelného zdroje od testovaného systému, | - | iradiance UVA (v mW/cm2) při této vzdálenosti, | - | doba expozice UV/VIS záření, | - | dávka záření UVA (iradiance x čas) v J/cm2, | - | teplota buněčných kultur během ozařování a kultur souběžně uchovávaných v temnu. Podmínky pokusu (d) - test NRU: |
- | složení média s NR, | - | doba inkubace s NR, | - | inkubační podmínky (koncentrace CO2, teplota, vlhkost), | - | podmínky extrakce NR (extrakční činidlo, doba extrakce), | - | vlnová délka, při které se spektrofotometricky odečítala optická hustota NR, | - | druhá vlnová délka (referenční), byla-li použita, | - | složení srovnávacího roztoku pro spektrofotometrii (blanku), pokud byl použit. Výsledky: |
- | životaschopnost buněk při jednotlivých koncentracích testované látky, vyjádřená v procentech vůči průměrné životaschopnosti kontrol, | - | křivky - koncentrace-odezva (koncentrace testované látky vs relativní životaschopnost buněk) získané souběžnými experimenty +UVA a -UVA, | - | analýza křivek koncentrace-odezva: podle možnosti výpočet hodnot EC50 (+UVA) a EC50 (-UVA), | - | porovnání obou křivek koncentrace-odezva získaných za použití ozařování UV/VIS světlem - výpočtem buď fotoiritačního faktoru (PIF) nebo středního fotoefektu (MPE), | - | klasifikace fototoxického potenciálu, | - | kritéria akceptovatelnosti testu (a) - souběžná negativní kontrola: | - | absolutní životaschopnost (optická denzita extraktu NR) ozářených a neozářených buněk, | - | historické údaje negativních kontrol, průměr a směrodatná odchylka, | - | kritéria akceptovatelnosti testu (b) - souběžná pozitivní kontrola: | - | hodnoty EC50 (+UVA), EC50 (-UVA) a PIF látky použité pro pozitivní kontrolu, | - | historické údaje látky použité pro pozitivní kontrolu: hodnoty EC50 (+UVA), EC50 (-L)VA) a PIF, průměry a směrodatné odchylky. Diskuse výsledků. Závěry. |
Dodatek Úloha testu fototoxicity 3T3 NRU v sekvenčním přístupu k testování fototoxicity látek 
|